Pacientiem ar tuberkulozi vispārējās asins analīzes izmaiņas nav patognomoniskas. Ar ierobežotiem un neaktīviem tuberkulozes veidiem, parastajam numuram ir raksturīga eritrocītu hipohromija. Ar masveida infiltrātiem vai kazeozu pneimoniju, plaši izplatītu kaulu limfadenītu, ir konstatēti specifiski zarnu bojājumi, kā arī liela plaušu vai pēcoperācijas asiņošana, eritropēnija un mikrocitoze, oligohromasija, polihromasija. Makrocitoze, un vēl jo vairāk, poikilocitoze ir daudz retāka, parasti ar smagu anēmiju. Retikulocītu skaits ar kompensētu tuberkulozes stadiju svārstās no 0,1 līdz 0,6% ar subkompensētu, no 0,6 līdz 1,0% un 1% retikulocītu ir raksturīgi dekompensētiem.
Tuberkulozes gadījumā var novērot mērenu leikocitozi (līdz 15 tūkstošiem leikocītu), retāk leikopēniju, kas notiek 2-7% gadījumu pacientiem ar ierobežotu un viegli progresējošu procesu formu un 12,5% - ar destruktīvu un progresējošu plaušu tuberkulozi. .
Visbiežāk notiek izmaiņas leikocītu formā. Gan relatīvā, gan absolūtā neitrofīlija, mērena leikocītu nobīde pa kreisi līdz promielocītiem. Meliocīti ir ļoti reti sastopami nekomplicētu tuberkulozes gadījumā. Neitrofilu ar patoloģisku smilšu skaita pieaugums pacienta, kam ir tuberkuloze, hemogrammā vienmēr norāda procesa ilgumu: pacientiem ar smagu tuberkulozi gandrīz visi neitrofili satur patoloģisku smilšu. Kad tuberkulozes uzliesmojums izzūd, kodolieroču maiņa nonāk normāli salīdzinoši ātri. Neitrofilu nenormāla granularitāte parasti ilgst ilgāk nekā citas izmaiņas hemogrammā.
Lielākā daļa primārās tuberkulozes formas ir saistīta ar limfopēniju, ko dažkārt novēro pat vairākus gadus pat pēc īpašām izmaiņām. Sekundārā tuberkuloze akūtajā fāzē atkarībā no procesa smaguma var būt saistīta ar normālu limfocītu skaitu vai limfopēniju.
No tuberkulozes procesa novērtēšanas testiem īpaša vieta ir eritrocītu sedimentācijas ātruma (ESR) noteikšana, kas ir svarīga tuberkulozes procesa gaitas novērtēšanai un tās aktīvo formu noteikšanai. ESR pieaugums liecina par patoloģiska procesa (infekcijas-iekaisuma, strutainas, septiskas, hemoblastozes, Hodžkina slimības uc) klātbūtni un kalpo par tās smaguma rādītāju, tomēr parastie ESR indikatori ne vienmēr norāda uz patoloģijas trūkumu. Eritrocītu nogulsnēšanos paātrina globulīnu, fibrinogēna, holesterīna un asins viskozitātes samazināšanās asinīs. Eritrocītu sedimentācijas palēnināšanās ir raksturīga apstākļiem, kam seko hemoconcentrācija, albumīna un žultsskābes satura palielināšanās.
Hemogramma pacientiem ar tuberkulozi ārstēšanas laikā mainās. Hematoloģiskās izmaiņas izzūd ātrāk, jo veiksmīgāka ir terapeitiskā iejaukšanās. Tomēr jāņem vērā dažādu antibakteriālo zāļu ietekme uz asinsradi. Viņi bieži izraisa eozinofiliju, dažos gadījumos - leikocitozi un biežāk leikopēniju līdz agranulocitozei un limfoid-retikulārai reakcijai. Sistemātiska hematoloģiskā kontrole un iegūto datu pareiza analīze ir būtiski, lai novērtētu pacienta klīnisko stāvokli, procesa dinamiku un pielietotās ārstēšanas efektivitāti.
Urīna analīze
Urīnceļu tuberkulozes gadījumā urīna testēšana ir galvenā laboratorijas diagnostikas metode. Var novērot leikocitūriju, eritrocitūriju, proteinūriju, hipoisostūriju, tuberkulozi mikobaktēriju, nespecifisku bakteriūriju.
Leukocitūrija ir visizplatītākais urīnceļu sistēmas tuberkulozes simptoms pirms specifiskas ķīmijterapijas, un tas nav pieejams tikai izņēmuma gadījumos, piemēram, ar urētera lūmena pilnīgu iznīcināšanu. Nechiporenko tests (leikocītu skaita noteikšana 1 ml urīna) palīdz objektīvāk novērtēt leikocitūrijas pakāpi nefrotuberkulozē un dažos gadījumos to identificēt normālā urīna analīzē. Tomēr jāatceras, ka leikocitūrija var būt akūta un hroniska pielonefrīts, cistīts, uretrīts, akmeņi nierēs un urīnceļos.
Eritrocitūrija. kā leikocitūrija. Tā tiek uzskatīta par vienu no visbiežāk sastopamām urīnizvadkanāla tuberkulozes laboratoriskajām pazīmēm. Hematūrijas biežums ir atkarīgs no procesa izplatības, tas palielinās līdz ar destruktīvas tuberkulozes procesa attīstību nierēs. Eritrocitūrija bez leikocitūrijas ir raksturīgāka nieru tuberkulozes agrīnajām stadijām. Hematūrija, kas dominē pār leikocitūriju, ir svarīgs arguments par labu nieru tuberkulozei tās diferencēšanā ar nespecifisku pielonefrītu.
Bioķīmiskā asins analīze
Tuberkulozes gadījumā dažu bioķīmisko parametru izmaiņas galvenokārt ir atkarīgas no procesa fāzes, komplikācijām un dažādām līdzīgām slimībām. Pacientiem ar neaktīvu plaušu un citu orgānu tuberkulozi asins seruma kopējā olbaltumvielu un olbaltumvielu frakcija nemainās un nosaka to normālu saturu.
Akūtās slimības formās, kā arī hronisku tuberkulozes formu saasināšanā un progresēšanā albumīna globulīna koeficients samazinās.
Lai novērtētu tuberkulozes un tā komplikāciju funkcionālo stāvokli un organiskos bojājumus aknās, ir svarīgi noteikt tiešā un kopējā bilirubīna, aspartāta aminotransferāzes (ACT), alanīna aminotransferāzes (ALT) līmeni serumā. Aminotransferāžu līmeņa dinamiskā noteikšana. bilirubīns pacientu ar tuberkulozi ārstēšanā, īpaši tās smagajās formās, ir obligāta sastāvdaļa tuberkulozes pacientu bioķīmiskajā pārbaudē un tiek veikta katru mēnesi.
Nieru funkcionālā stāvokļa novērtējums ietver seruma kreatinīna noteikšanu un glomerulārās filtrācijas ātruma aprēķināšanu, izmantojot Cockroft-Gault formulu. Glomerulārās filtrācijas ātruma aprēķināšana, izmantojot Reberg testu, dod mazāk precīzus rezultātus.
Galvenais mērķis dinamisko bioķīmisko pētījumu veikšanai pacientiem ar tuberkulozi ir kontrolēt procesa gaitu, savlaicīgi identificēt zāļu blakusparādības un atbilstošu homeostāzes traucējumu korekciju.
Bioķīmisko pētījumu metožu izmantošana ekstrapulmonālajā tuberkulozē
Informatīvākais rādītājs ņem vērā tuberkulostearīnskābes saturu bioloģiskajos šķidrumos, bet tā definīcija ir saistīta ar tehniskām grūtībām (nepieciešamību izmantot gāzes hromatogrāfiju un masas spektrometriju).
Daudzsološs ir izmērīt adenozīna deamināzes - fermenta, kas tiek konstatēts šķidrumos: sinoviālā, perikarda, ascitiskā vai cerebrospinālā - aktivitāti. Galvenie adenozīna dinazāzes ražotāji ir limfocīti un monocīti. Adenozīna deamināzes aktivitātes noteikšana bioloģiskajos šķidrumos atvieglo tuberkulozes sinovīta, limfmezglu tuberkulozes, tuberkuloza meningīta, tuberkulozes serozīta diagnozi.
Daži bioķīmiskie parametri to specifiskuma dēļ tiek noteikti tikai bioloģiskajos šķidrumos, kas atrodas tuvu bojājumam. Rādītāju līmeni mēra, reaģējot uz subkutānu vai intrakutālu tuberkulīna ievadīšanu (parasti pirms ievadīšanas un 48 un 72 stundas pēc tās). Pēc tam tiek aprēķināts marķiera līmeņa pieauguma līmenis (%) attiecībā pret sākotnējo līmeni.
Optimāls orgānu specifiskā enzīma transamidināzes aktivitātes noteikšana urīnā, kura izskats tiek konstatēts ar dažāda veida nieru bojājumiem. Transaminidāzes pētījums ir pamatots tikai tuberkulīna subkutānas ievadīšanas apstākļos, lai pastiprinātu lokālo iekaisuma procesu. Transamidināzes aktivitāte urīnā tiek noteikta sākumā un 24-72 stundas pēc 50 TE tuberkulīna ievadīšanas. Fermenturijas palielināšanās par 2 un vairāk reizes ļauj 82% gadījumu diferencēt nieru aktīvo tuberkulozi no hroniskas pielonefrīta saasināšanās.
Sieviešu dzimumorgānu tuberkulozē haptoglobīna un malondialdehīda koncentrācija asinīs tiek noteikta provokatīvā tuberkulīna testā. Tuberkulīnu ievada subkutāni ar devu 50 TE, un pēc 72 stundām veic atkārtotu bioķīmisko pētījumu. Tuberkulozes etioloģijas gadījumā haptoglobīna līmeņa paaugstināšanās pakāpe ir vismaz 28% un malondialdehīda līmenis - 39% vai vairāk. Tiek izmantota arī adenozīna deamināzes aktivitātes definīcija peritonālajā šķidrumā, kas iegūts no Douglas telpas. Punktu atkārtoti pārbauda 72 stundas pēc tuberkulīna intradermālas ievadīšanas 0,1 TE un 0,01 TE devās iekšējo dzimumorgānu projekcijas zonā uz priekšējās vēdera sienas. Par labu tuberkulozes procesam, adenozīna deamināzes aktivitātes pieaugums par 10% vai vairāk, salīdzinot ar sākotnējo, ir indikatīvs.
Ar acu bojājumiem tiek pārbaudīta fokusa reakcija, kas rodas acī, reaģējot uz antigēnu stimulāciju. Tajā pašā laikā nevēlamas izteiktas reakcijas attīstība kopā ar vizuālo funkciju samazināšanos. Tā kā minimālo fokusa reakciju novērtēšana bieži ir sarežģīta, lai objektīvi novērtētu secinājumu, ieteicams paralēli koncentrēties uz haptoglobīna vai adenozīna deamināzes pieauguma pakāpi.
Visi bioķīmiskie pētījumi jāveic kopā ar citām metodēm.
Asins koagulācijas tests
Asins koagulācijas sistēmas stāvokļa pētījuma nozīmīgums fhtisioloģijā ir saistīts ar hemorāģiju vai plaušu asiņošanu klīniskajos tuberkulozes slimnieku skaitā, kā arī hemocoagulācijas komplikācijām tuberkulozes ķirurģiskajā ārstēšanā. Turklāt latentā intravaskulārā hemocoagulācija, kas pastāvīgi saistīta ar tuberkulozi, ietekmē slimības gaitu un ķīmijterapijas efektivitāti.
Pacientiem ar plaušu tuberkulozi, kurā dominē iekaisuma eksudatīvā komponente, novēro asins antikoagulanta aktivitātes samazināšanos. Pacientiem ar nelielu specifisku bojājumu izplatību plaušās ar iekaisuma produktīvās sastāvdaļas pārsvaru, intravaskulārā hemocoagulācija nav ļoti izteikta. Pacientiem ar plaušu tuberkulozi ar hemoptīzi un plaušu asinsizplūdumiem asins koagulācijas sistēma ir atšķirīga: pacientiem ar nelielu asins zudumu hemoptoe augstumā vai tūlīt pēc tās izbeigšanās novēro strauju asins koagulācijas pieaugumu sakarā ar izteiktu trombīna veidošanās procesu pastiprināšanos, saglabājot palielinātu "strukturālo" asins pietūkumu. Pacientiem ar masveida asins zudumu novērota koagulācijas potenciāla samazināšanās fibrinogēna koncentrācijas samazināšanās dēļ. XIII faktora aktivitāte, trombocītu skaits. Ķirurģiskās ārstēšanas stadijā pacientiem ar ierobežotām plaušu tuberkulozes formām nav nozīmīgu traucējumu ar homeostāzes sistēmu. Pacientiem ar kopīgiem procesiem, veicot pneimonīmu vai pleuropneumonektomiju, bieži rodas DIC, kas var būt „otrās slimības” forma.
Lai kontrolētu asins koagulācijas sistēmas stāvokli pacientiem ar plaušu tuberkulozi, nepieciešams noteikt aktivēto daļējo tromboplastīna laiku (APTT), fibrinogēnu, trombīna laiku, protrombīna indeksu, kā arī asiņošanas laiku un asinsreces laiku.
Hormonālie pētījumi
Mūsdienu eksperimentālie un klīniskie novērojumi liecina par specifiskas plaušu pneimonijas hormonālās stadijas izmaiņām. Pierādīts, ka hipofīzes-virsnieru, hipofīzes-vairogdziedzera sistēmu un aizkuņģa dziedzera funkcijas disfunkcijas korekcija saistībā ar anti-tuberkulozes terapiju veicina fibrogēzes procesu aktivizēšanu un remontu specifiskā iekaisuma centrā.
Hipofīzes-vairogdziedzera sistēmas funkcionālo stāvokli nosaka pēc trijodironīna (T 3), tiroksīna (T 4), vairogdziedzera stimulējošā hipofīzes hormona (TSH) satura. Ir konstatēts, ka 38–45% pacientu ar plaušu tuberkulozi tiek konstatēta subklīniska hipotireoze, un visbiežāk tā ir diagnosticēta izplatītajos un fibro-dobos procesos. Ar šīm pašām formām gan T3, gan T4 līmeņi ir visstraujāk samazināti, un šo hormonu nelīdzsvarotība rodas, palielinot attiecību T 4 / T h.
Virsnieru garozas funkciju novērtē ar kortizola līmeni asins serumā un aizkuņģa dziedzera endokrīno funkciju pēc imūnreaktīvā insulīna koncentrācijas. Infekcijas slimības akūtajā fāzē palielinās endogēnā kortizola un insulīna nepieciešamība. Hiperinsulinēmija norāda arī uz ķermeņa audu insulīna rezistenci, kas ir raksturīga jebkuram aktīvam iekaisuma procesam, īpaši specifiskam. Ar aknu plaušu tuberkulozi saistītu virsnieru dziedzeru glikokortikoīdu funkcijas noteikšana vairumā pacientu atklāj hiperkorticisma klātbūtni. Parastie kortizola koncentrācijas rādītāji pacientiem ar infekciozu iekaisumu akūtā periodā ir jāuzskata par virsnieru garozas glikokortikoīdu funkcijas relatīvo nepietiekamību, kas var kalpot par pamatu aizstājterapijai ar atbilstošām glikokortikoīdu devām.
Gandrīz trešdaļu pacientu ar plaušu tuberkulozi var konstatēt, ka viņu insulīna līmenis ir diezgan zems un tuvojas normas zemākajai robežai, savukārt 13-20% ir nozīmīgs hiperinsulinisms. Gan relatīvais hipo, gan hiperinsulinisms ir augsti riska faktori, kas rada dažāda smaguma ogļhidrātu vielmaiņas traucējumu attīstību. Šīs aizkuņģa dziedzera B šūnu funkcionālās aktivitātes izmaiņas prasa regulāru glikēmijas kontroli pacientiem ar tuberkulozi un savlaicīgu diabēta profilaksi. Turklāt. tas kalpo kā papildu pamatojums insulīna fizioloģisko devu izmantošanai kompleksajā tuberkulozes terapijā.
Kopumā vairogdziedzera hormonu līmeņa samazināšanās, to nelīdzsvarotība, hipercortisolēmija un hiperinsulinisms ir visizteiktākie pacientiem ar smagu tuberkulozi, ar plašu plaušu bojājumu un smagiem tuberkulozes intoksikācijas simptomiem.
Tuberkulozes mikrobioloģiskā diagnoze
Mikrobioloģiskie pētījumi ir nepieciešami, lai identificētu pacientus ar tuberkulozi, pārbaudītu diagnozi, pārraudzītu un koriģētu ķīmijterapiju, novērtētu ārstēšanas rezultātus, citiem vārdiem sakot, no pacienta reģistrācijas ar tuberkulozi līdz izņemšanai no reģistra.
Visas epidemioloģiskās programmas un projekti ir balstīti uz aprēķināto baktēriju ekskrementu skaitu, ko nevar izdarīt, neizmantojot laboratorijas metodes mikobaktēriju tuberkulozes noteikšanai. Pārbaudot tā saukto neorganizēto iedzīvotāju apgrozāmību, baktēriju izdalīšanās procentuālais daudzums sasniedz 70 vai vairāk, kas padara laboratorijas metodes par diezgan efektīvu līdzekli, lai identificētu šīs grupas pacientus ar tuberkulozi.
Tradicionālās mikrobioloģiskās metodes tuberkulozes diagnostikai - bakterioskopiskas un kultūras studijas. Mūsdienu metodēs tiek apsvērta mikobaktēriju tuberkulozes audzēšana automatizētās sistēmās, PCR. Tomēr visas šīs metodes noteikti ir apvienotas ar klasiskajām bakterioloģiskajām metodēm.
Diagnostikas materiālu vākšana
Laboratorijas testu efektivitāte lielā mērā ir atkarīga no diagnostiskā materiāla kvalitātes. Diagnostikas materiāla savākšanas, uzglabāšanas un transportēšanas noteikumu ievērošana un pacientu izmeklēšanas algoritma precīza izpilde tieši ietekmē rezultātu un nodrošina bioloģisko drošību.
Tuberkulozes pētījumiem, izmantojot dažādus materiālus. Sakarā ar to, ka plaušu tuberkuloze ir visbiežāk sastopamais tuberkulozes bojājumu veids, krūts un citi tracheobronhijas koku sekrēciju veidi tiek uzskatīti par galvenajiem pētījuma materiāliem: augšējo elpceļu izvadīšana pēc aerosola ieelpošanas: bronhu skalošanas ūdens; bronhokalveolārie skalošanas līdzekļi; materiāls, ko iegūst, izmantojot bronhoskopiju, transtrāzi un intrapulmonālo biopsiju: aspirēt no bronhiem, balsenes uztriepēm, eksudātiem, smērēm no brūcēm utt.
Pētījumu efektivitāte palielinās, ja viņi veic kontrolētu materiālu savākšanu no pacienta. Lai to izdarītu, piešķiriet speciāli aprīkotu telpu vai iegādājieties īpašas kajītes. Materiālu vākšana ir bīstama procedūra, tāpēc jums ir nepieciešams savākt materiālus pētniecībai, ievērojot infekcijas drošības noteikumus.
Mikrobakteriju tuberkulozes izpētes materiāls tiek savākts sterilos flakonos ar cieši aizskrūvētiem vāciņiem, lai novērstu vides piesārņojumu un aizsargātu savākto materiālu no piesārņojuma.
Flakoniem diagnostikas materiāla savākšanai jāatbilst šādām prasībām:
- jābūt izgatavotiem no triecienizturīga materiāla;
- vajadzētu viegli izkausēt, autoklāvējot;
- jābūt pietiekamam tilpumam (40-50 ml):
- ir plaša krēpu atvērums (diametrs nav mazāks par 30 mm);
- jābūt viegli lietojamiem, caurspīdīgiem vai caurspīdīgiem, lai jūs varētu novērtēt savāktā parauga daudzumu un kvalitāti, neatverot vāku.
Lai iegūtu optimālus pētījumu rezultātus, jāievēro šādi nosacījumi:
- materiālu savākšana notiek pirms ķīmijterapijas sākuma;
- pētījuma materiāls jāsavāc pirms pārtikas un narkotiku uzņemšanas no rīta;
- pētījumiem ir vēlams savākt vismaz trīs rīta krēpu paraugus. Savākt krēpu 3 dienas pēc kārtas;
- savāktais materiāls jāpiegādā laboratorijā pēc iespējas ātrāk:
- ja nav iespējams nekavējoties nogādāt materiālu uz laboratoriju, to uzglabā ledusskapī 4 ° C gaisa temperatūrā ne ilgāk kā 48 stundas;
- transportējot materiālu, rūpīgi jāuzrauga flakonu integritāte.
Pareizi savāktajam krēpam ir gļotādas vai mucopurulents raksturs. Izpētītās krēpu daļas optimālais tilpums ir 3-5 ml.
Flegma tiek savākta ārsta uzraudzībā. Personas, kas atbildīgas par krēpu vākšanu, ir jāpārrauga dažu noteikumu īstenošana:
- jums jāpaskaidro pacientam pētījuma mērķis un nepieciešamība klepus ne siekalām vai deguna gļotādām, bet dziļo elpceļu saturs. To var panākt, pateicoties produktīvam klepus, kas rodas pēc dažām (2-3) dziļa elpām. Ir arī jābrīdina pacients, ka viņam vispirms jāizskalo muti ar vārītu ūdeni, lai noņemtu galveno mutes dobuma mikrofloras daļu un pārtikas gruvešus, kas kavē krēpu izpēti;
- medicīniskajam darbiniekam, kas iesaistīts krēpu savākšanā, papildus drēbēm un vāciņam jāvalkā maska, gumijas cimdi un gumijas priekšauts;
- stāvot aiz pacienta, viņam ir ieteicams glabāt pudeli pēc iespējas tuvāk lūpām un nekavējoties sadalīt krēpu tajā, kamēr tas klepus, bet ir nepieciešams nodrošināt, lai gaisa plūsma tiktu novirzīta no veselības aprūpes sniedzēja:
- pēc krēpu savākšanas pabeigšanas ārstam ir rūpīgi jāaizver flakons ar vāciņu un jānovērtē savākto krēpu daudzums un kvalitāte. Tad pudele tiek marķēta un ievietota speciālā biksā transportēšanai uz laboratoriju.
Ja pacients neizdala krēpu, tad nakts pirms un agri no rīta materiāla savākšanas dienā jādod atkrēpošanas līdzeklis: Altea zāļu saknes ekstrakts (mukaltīns), bromheksīns, ambroksols uc - vai uzlikt kairinošu ieelpojumu, izmantojot iekārta, kas uzstādīta savākšanas telpā. krēpas Šādā veidā savāktie materiāli nevar tikt saglabāti un jāpārbauda savākšanas dienā. Lai izvairītos no viņa "noraidīšanas" laboratorijā virzienā, būtu jāizveido īpaša zīme.
Ja šajā iestādē neveic mikrobioloģiskos pētījumus, savākto diagnostikas materiālu centralizēti nogādā laboratorijā, ja materiāls ir obligāti jāsaglabā starp piegādēm ledusskapī vai ar konservantiem. Materiāls tiek nogādāts laboratorijā transporta kastēs, kuras var viegli dezinficēt. Katram paraugam jābūt marķētam ar atbilstošu etiķeti, un visa partija jāaizpilda kopā ar pievienoto veidlapu.
Pacientu izmeklēšanas veidi un biežums
Sākotnējā, tā sauktās diagnostikas, pacienta tuberkulozes izmeklēšanas laikā ir jāpārbauda vismaz 3 poras poru 2 vai 3 dienu laikā. apkopoti medicīnas darbinieku uzraudzībā, kas palielina mikroskopijas efektivitāti.
Primāro tuberkulozes skrīningu veic visas veselības sistēmas medicīniskās diagnostikas iestādes. Nesen, lai palielinātu primārās pārbaudes efektivitāti, ir izveidoti tā saucamie mikroskopijas centri, kas balstīti uz klīniskās diagnostikas laboratorijām un aprīkoti ar moderniem mikroskopiem un aprīkojumu epidēmijas drošības nodrošināšanai.
TB objektos tiek izmantots skrīninga grafiks, kas ietver krēpu vai citu diagnostikas materiālu izpēti vismaz 3 reizes 3 dienu laikā. Ārstēšanas procesā mikrobioloģiskie pētījumi tiek veikti regulāri vismaz reizi mēnesī intensīvas ķīmijterapijas fāzē. Pārejot uz turpmāko posmu, pētījumi tiek veikti retāk - ar 2-3 mēnešu intervālu, bet pētījumu daudzveidība ir samazināta līdz diviem.
Diagnostiskā materiāla savākšanas iezīmes ekstrapulmonālajā tuberkulozē
Patoloģiskā materiāla īpatnība tuberkulozes ekstrapulmonārajās formās ir neliela mikobaktēriju tuberkulozes koncentrācija tajā, kas prasa jutīgākas mikrobioloģiskās izpētes metodes, pirmkārt, metodes barošanas vidē.
Urogenitālās tuberkulozes gadījumā urīns ir vispieejamākais pētniecības materiāls. Urīna paraugu ņemšanu veic apmācīta medmāsa.
Ārējās dzimumorgānus mazgā ar ziepēm un ūdeni vai vāju kālija permanganāta šķīdumu. Uzmanīgi apstrādājiet urīnizvadkanāla ārējo atvērumu. Vidēja daļa no rīta urīna tiek savākta sterilā flakonā: vīriešiem - protams, sievietēm - ar katetru. Urīns no nieru iegurņa tiek savākts sterilās caurulēs, lai kateterizētu vienu vai divas nieres, pēdējā gadījumā - vienmēr atsevišķi no katras nieres. Neliels daudzums šīs urīna tiek centrifugēts, nogulsnes pārbauda.
Vīriešiem spermu, sēklinieku punkcijas, prostatas izdalījumus centrifugē, lai iegūtu nogulsnes. Jebkurā specifiskā procesa lokalizācijā vīriešu dzimumorgānā prostatas dziedzeru masāža var veicināt tuberkulozes mikobaktēriju sekrēciju.
Vīriešu menstruālā asinis tiek savāktas sūknējot vai izmantojot Kafka vāciņu. Iegūto materiālu atbrīvo no sarkanajām asins šūnām, mazgājot to ar destilētu ūdeni, kam seko centrifugēšana. Granulu pārbauda.
Izvadīšana no dzemdes kakla kanāla tiek savākta jebkurā Kafkas tvertnē vai vāciņā, tas ir, vēlams uzkrāt 1-2 ml patoloģiska materiāla.
Materiāls, kas iegūts operācijas laikā uz nierēm, dzimumorgāniem. biopsijas, skrāpējumi no endometrija, homogenizēti. Lai to izdarītu, to ievieto sterilā javas un rūpīgi sasmalcina ar sterilām šķērēm. Iegūtajai suspensijai pievieno sterilu upes smilšu daudzumu, kas ir vienāds ar tā masu, pēc tam pievieno 0,5-1,0 ml izotoniskā nātrija hlorīda šķīduma un sasmalcina visu, līdz tiek veidota masveida masa, pievienojot izotonisku nātrija hlorīda šķīdumu (4-5 ml). Tad masai ļauj nokristies 1-1,5 minūtes, pārbauda supernatantu.
Kaulu un locītavu tuberkuloze. Punktu (abscesu abscesu pūce), kas iegūta ar sterilu šļirci, ievieto sterilā traukā un nekavējoties nogādā laboratorijā. Sterils pipete, kas iepriekš samitrināta ar sterilu izotonisku nātrija hlorīda šķīdumu, ieņem 2-5 ml strutas, pārnes to uz pudelēm ar pērlītēm un pievieno vēl 2-3 ml izotoniskā nātrija hlorīda šķīduma. Pudelīte tiek aizvērta ar aizbāzni un joks aparātā krata 8-10 minūtes. Pārbauda homogenizēto suspensiju.
Par osteo-locītavu tuberkulozes fistulālajām formām no fistulas tiek ņemts strutas. Liela izlāde tiek savākta tieši mēģenē. Nepietiekamas izplūdes gadījumos fistulas gājiens tiek nomazgāts ar sterilu izotonisku nātrija hlorīda šķīdumu, un testa ūdenī savāktie mazgāšanas ūdeņi vai tampona gabals, kas iemērkts strūklā, tiek nosūtīti pārbaudei.
Ķirurģiskie materiāli, kas iegūti operācijas laikā uz kauliem un locītavām, var sastāvēt no strutainām nekrotiskām masām, granulācijām, rētām, kaulu audiem, sinovialo membrānu audiem un citiem substrātiem. To apstrādā kā nieru tuberkulozi.
Sintētiskā šķidruma mikrobioloģiskā pārbaude 3% nātrija citrāta šķīdumā (attiecība 1: 1), lai novērstu recēšanu, tiek veikta tieši pēc punkcijas.
Limfmezglu tuberkuloze. Tika pārbaudīta arī limfmezglu punkcijas laikā iegūta strūkla. kā zarnu abscesu pūce. Limfmezglu audus, kas iegūti operācijas laikā, biopsijas, pārbauda tāpat kā ar citiem tuberkulozes veidiem.
Pētījums par mikobaktēriju tuberkulozes izkārnījumu masām ir ļoti reti, jo pozitīvie rezultāti gandrīz nav pilnīgi.
Mikroskopijas mikobaktērijas
Krēpu mikroskopija ir samērā ātra, vienkārša un lēta metode, kas jāizmanto visos iespējamos tuberkulozes gadījumos. Turklāt šis pētījums tiek veikts, lai novērtētu ķīmijterapijas efektivitāti un konstatētu atveseļošanos vai neveiksmīgu ārstēšanas rezultātu bez kultūras rezultātiem.
Izmantot divas mikroskopiskās pārbaudes metodes:
- tiešā mikroskopijas metode, kad uztriepes tiek gatavotas tieši no diagnostikas materiāla;
- nogulumu mikroskopijas metode, kas sagatavota no dekontaminēta materiāla kultūrai.
Pirmo metodi izmanto laboratorijās, kurās veic tikai mikroskopiskus izmeklējumus (vispārējās medicīnas tīkla klīniskās diagnostikas laboratorijas).
Labākos mikroskopiskos izmeklējuma rezultātus iegūst, koncentrējot diagnostisko materiālu (piemēram, centrifugējot).
Lai noteiktu mikobaktēriju tuberkulozi ar 50% mikroskopijas iespējamību, 1 ml krēpu satur vairāk nekā 5000 mikrobu šūnas. Pacientu flegma ar plaušu formas Tuberkuloze parasti satur ievērojamu daudzumu skābju rezistentu baktēriju, kas ļauj droši noteikt tos mikroskopijas laikā. Šīs metodes diagnostisko jutīgumu var uzlabot, pārbaudot vairākus krēpu paraugus no viena pacienta. Negatīva bakterioskopija neizslēdz tuberkulozes diagnozi, jo dažu pacientu krēpās ir mazāk mikobaktēriju, nekā to var noteikt ar mikroskopu. Sliktas krēpu uztriepes sagatavošana var būt arī negatīvas bakterioskopiskas pārbaudes cēlonis.
Visbiežāk izmantotā metode skābju rezistentu mikobaktēriju noteikšanai uztriepēs ir krāsošana saskaņā ar Ziehl-Nelsen. Šī metode ir balstīta uz karbola fuksīna iekļūšanu mikrobu šūnā caur membrānu, kas ietver vaska lipīdu slāni, vienlaicīgi iedarbojoties uz karsēšanu un spēcīgu fenola kodināšanas efektu. Sekojoša uztriepes krāsas maiņa ar 25% sērskābes šķīdumu vai 3% sālsskābes spirtu izraisa visu ne-skābes izturīgu struktūru krāsas maiņu. Krāsu izlīdzinošie elementi tiek krāsoti ar 0,3% metilēnzilā šķīdumu. Mikobaktērijas neuzskata parastās anilīna krāsvielas, kā rezultātā skābju rezistentās mikobaktērijas ir krāsotas aveņu sarkanā krāsā, un citi mikrobi un šūnu elementi - zilā krāsā.
Zilu-Nelsenā iekrāsoto uztriepju pārbaudei tiek izmantots viegls binokulārais mikroskops ar iegremdēšanas mērķi (90 vai 100 reižu palielinājums) un okulārs ar 7 vai 10 reižu palielinājumu. Izpētīt 100 redzes laukus, kas ir pietiekami, lai identificētu uztriepju vienu mikobaktēriju. Ja šāda pētījuma rezultāts ir negatīvs, apstiprināšanai ieteicams apskatīt vēl 200 redzes laukus. Reģistrē rezultātus, norādot atklāto skābju rezistentu mikobaktēriju skaitu (CUM).
Papildus šai metodei luminiscences mikroskopijai tiek izmantoti fluorohromi, kas ļauj sasniegt labākos rezultātus. Šīs metodes izmantošana palielina mikroskopijas efektivitāti par 10-15%. Apstrādājot mikobaktēriju ar luminiscējošām krāsvielām (auramīnu, rodamīnu utt.), Šīs vielas ir saistītas arī ar vaska līdzīgām mikrobu šūnu struktūrām. Kad krāsota šūna tiek apstarota ar aizraujošu gaismas avotu (noteiktu ultravioletā starojuma spektru), tie sāk mirdzēt oranžu vai spilgti sarkanu gaismu uz melna vai tumši zaļa fona. Sakarā ar redzamā attēla lielo spilgtumu un kontrastu, jūs varat samazināt mikroskopa kopējo palielinājumu par 4-10 reizēm, kas paplašina redzes lauku un samazina preparāta skatīšanās laiku. Līdz ar to, pateicoties daudz lielākam lauka dziļumam, var palielināt pētījuma komfortu.
Lietojot fluorescences mikroskopu, ir nepieciešams daudz mazāk laika, lai aplūkotu to pašu uztriepes laukumu, nekā ar mikroskopiju, kas ir notraipīta ar Tsil-Nelsen. Ja darba dienas laikā mikroskopists izskata aptuveni 20-25 šādas uztriepes, tad izmantojot fluorescences mikroskopu, viņš var vienlaikus pārbaudīt vairāk nekā 60-80 paraugus. Pieredzējuši mikroskopi zina, ka šūnu krāsošana ar auramīna un rodamīna maisījumu kaut kādā veidā ir raksturīga skābju rezistentām mikobaktērijām, kas šajā gadījumā ir zelta stienīšu izskats. Saprofīti ir krāsaini zaļgani.
Vēl viena nozīmīga fluorescences mikroskopijas metodes priekšrocība ir spēja noteikt modificētas mikobaktērijas, kas zaudējušas vairākus nelabvēlīgus faktorus, īpaši intensīvu ķīmijterapiju, skābes rezistences īpašību un nav konstatētas šajā sakarā, kad tās ir iekrāsotas ar Tsil-Nelsen.
Fluorescences mikroskopijas trūkumi ietver salīdzinoši augstās mikroskopa izmaksas un tās darbību. Tomēr centralizētās vai citās lielās laboratorijās, kur slodze pārsniedz 3 tehniķu skaitu, kas strādā ar trim parastajiem mikroskopiem, ir lētāk izmantot vienu fluorescences mikroskopu.
Bakterioskopiskām metodēm ir samērā augsta specifitāte (89-100%). Aptuveni 97% pozitīvo rezultātu, kas iegūti ar jebkuru mikroskopijas metodi, nepārprotami apstiprina sēšanas rezultāti.
Jāatzīmē, ka patoloģiska materiāla uztriepes mikroskopiskā pārbaude nevar noteikt identificēto skābju rezistentu mikobaktēriju sugu. Mikroskopijas metode ļauj izteikt viedokli tikai par skābju rezistentu mikroorganismu klātbūtni vai neesamību preparātā, kas izskaidrojams ar to, ka ir liels skaits tuberkulozes ne-tuberkulozes skābju rezistentu mikroorganismu, kas ir morfoloģiski līdzīgi mikobaktērijām.
Puskvantitatīvās vienībās iegūto mikroskopijas rezultātu novērtējums.
Lai varētu salīdzināt dažādu mikroskopijas metožu rezultātus, tiek ieviesti empīriskie koeficienti. Piemēram, lai salīdzinātu ar fluorescējošām krāsām uzkrītošās uztriepes rezultātus ar gaismas mikroskopijas datiem (1000x palielinājums), ir nepieciešams sadalīt skābju rezistentu mikobaktēriju skaitu, kas konstatēts ar fluorescējošu mikroskopu, ar atbilstošo koeficientu, izmantojot 250 mikroskopa palielinājumu - 10, ar 450 reizes - 4, ar 630 reizes - pie 2.
Mikroskopijas iezīmes ekstrapulmonālajā tuberkulozē
Tiek veikta tieša mikroskopija, kā arī smērēšanas mikroskopija, kas sagatavota pēc bagātināšanas, kam seko Zill-Nelsen krāsošana vai luminiscences krāsvielas. Tiešā uztriepes mikroskopija ir neefektīva sakarā ar zemu mikobaktēriju koncentrāciju materiālā, un tāpēc ir racionālāk izmantot bagātināšanas metodes. Centrifugēšana ir visefektīvākā. Ja bioloģiskais materiāls ir viskozs, centrifugēšana tiek veikta ar vienlaicīgu homogenizāciju un materiāla sašķidrināšanu, kas tiek veikta, izmantojot ātrgaitas centrifūgas ar centrbēdzes spēku 3000 g un hipohlorīta šķīdumiem. Citas bioloģiskās bīstamības aerosolu veidošanās dēļ pašlaik netiek izmantotas citas bagātināšanas metodes, piemēram, mikrofotēšana.
Kultūras metode tuberkulozes diagnostikai
Sēšanas metode vai kultivēšanas metode ir jutīgāka nekā uztriepes mikroskopija, un tai ir vairākas priekšrocības salīdzinājumā ar pēdējo. Tas ļauj izpētīt vairākus desmitus dzīvotspējīgu mikobaktēriju pētītajā materiālā un tam ir liela diagnostiskā vērtība. Tas ir īpaši svarīgi, pētot materiālus no nesen diagnosticētiem vai ārstētiem pacientiem, kas izdalās nelielā daudzumā mikobaktēriju.
Salīdzinot ar mikroskopiju, kultūras pētījums ļauj palielināt identificēto tuberkulozes pacientu skaitu par vairāk nekā 15-25%, kā arī pārbaudīt tuberkulozi vairāk agrīnā posmākad slimība joprojām ir labi ārstējama. Ļoti svarīga kultūras pētījumu priekšrocība ir iespēja iegūt patogēna kultūru, kuru var identificēt un pētīt saistībā ar zāļu jutīgumu, virulenci un citām bioloģiskām īpašībām.
Audzēšanas metožu trūkumi ietver to ilgumu (materiālu gaidīšanas laiks sasniedz 10 nedēļas). augstākas izmaksas, diagnostikas materiālu apstrādes sarežģītība.
Diagnostiskā materiāla apstrādes principi
Tradicionālās mikrobioloģiskās metodes nevar izmantot tuberkulozes pētījumos. Tas ir saistīts ar faktu. ka mikobaktēriju tuberkuloze aug ļoti lēni, un lielākā daļa klīnisko materiālu paraugu satur strauji augošus pirogēnus un putekļainus mikroorganismus, sēnītes. To straujais pieaugums uz bagātīgiem barības vielām kavē mikobaktēriju veidošanos un neļauj izolēt tuberkulozes izraisītāju, tādēļ pirms sējas diagnostikas materiāls ir pakļauts iepriekšējai apstrādei. Turklāt mikobaktērijas, kas izdalās no pacienta elpceļiem, parasti ieskauj liels daudzums gļotu, kas apgrūtina koncentrēšanos. Šajā sakarā, pirms sējas un citu līdzīgu materiālu sēšanas, ir nepieciešama to sašķidrināšana un attīrīšana.
Visiem mazgāšanas līdzekļiem un dekontaminantiem ir vairāk vai mazāk izteikta toksiska iedarbība uz mikobaktērijām. Kā rezultātā pārstrādes līdz 90% mikobaktēriju var nomirt. Lai saglabātu pietiekamu mikobaktēriju populācijas daļu, ir jāizmanto vieglas apstrādes metodes, kas, no vienas puses, ļauj apturēt strauji augošus pirogēnus un putekļainus mikroorganismus un, no otras puses, saglabāt materiālā esošo mikobaktēriju dzīvotspēju.
Atkarībā no materiāla, tā viendabīguma un piesārņojuma pakāpes, pirms sējas tiek izmantoti dažādi dezinfekcijas līdzekļi: krēpu - nātrija hidroksīda šķīdumam - 4%, trīs aizvietotu nātrija fosfāta šķīdumiem, 10%, benzalkonija hlorīda trinātrija fosfātam, NALC-NaOH (N-acetil-L-cisteīns) nātrija hidroksīds) ar galīgo NaOH koncentrāciju 1%, urīnam un citiem šķidriem materiāliem - sērskābes šķīdumu 3%, piesārņotiem paraugiem, tauku saturošiem materiāliem - skābeņskābes šķīdums līdz 5%. Turklāt dažos gadījumos izmantojiet fermentus, virsmaktīvās vielas (mazgāšanas līdzekļus). Dažu citu mazgāšanas līdzekļu lietošana ir saistīta ar mazāku mikobaktēriju šūnu nāvi (40-50% izdzīvo). tomēr tos var izmantot tikai šķidrajiem materiāliem. Visplašāk izplatītais pasaulē saņēma NALC-NaOH. izlaists komplektos. Šī metode ļauj izvēlēties vairāk nekā 85% mikobaktēriju šūnu populācijas. Audu saturošu cietu materiālu dekontaminācija ir sarežģītāka, jo ir grūti uzminēt materiāla dispersijas pakāpi homogenizācijas procesā. Piemēram, limfmezglu biopsijas paraugu apstrāde bieži vien ir saistīta ar paaugstinātu piesārņojuma biežumu ar svešām florām. Šajā gadījumā var izmantot 1% etoniju.
Nehomogēns materiāls tiek homogenizēts, izmantojot stikla lodītes dekontaminantu klātbūtnē. Šķidrie materiāli tiek iepriekš centrifugēti un tiek apstrādātas tikai nogulsnes.
Sēšanas un inkubācijas metodes
Pēc pirmapstrādes materiāls tiek centrifugēts, tāpēc mikobaktērijas tiek nogulsnētas un to saturs sedimentos palielinās (“sedimentu bagātināšana”). Iegūtās nogulsnes tiek pakļautas neitralizācijai un sēklas ar to (inokulē) blīvās barotnes virsmu vai mēģenes ar šķidrumu (daļēji šķidrumu). No pārējām nogulsnēm mikroskopiskai pārbaudei sagatavo uztriepes. Sēšanas metodei ir jānovērš diagnostiskā materiāla savstarpēja piesārņošana.
Mikrobioloģisko pētījumu rezultātu drošai klīniskai interpretācijai ir jāievēro šāds noteikums: mikroskopiskie un kultūras pētījumi jāveic paralēli no tā paša diagnostikas materiāla parauga.
Inokulētās caurules ievieto termostatā pie 37 o С 2 dienas horizontālā stāvoklī. Tas nodrošina vienmērīgāku materiāla uzsūkšanos barības vidē. Pēc 2 dienām caurules tiek novietotas vertikālā stāvoklī un hermētiski noslēgtas ar gumijas vai silikona aizbāžņiem, lai novērstu sēklas materiāla izžūšanu.
Kultūras, kas tiek turētas termostatā 37 ° C temperatūrā 10-12 nedēļas ar regulāru iknedēļas apskati. Katrā testa skatā tiek reģistrēti šādi parametri:
- vizuāli novērots no sējas augšanas dienas;
- pieauguma temps (CFU skaits);
- stādīšanas piesārņojums ar svešām mikrobu florām vai sēnēm (šādas caurules tiek noņemtas);
- nav redzamas izaugsmes. Caurules paliek termostatā līdz nākamajai apskatei.
Uzturvielu barotne
Mikobaktēriju audzēšanai, izmantojot dažādas barības vielas; blīvs, daļēji šķidrs, šķidrums. Tomēr nevienai no pazīstamajām barotnēm nav tādu īpašību, kas nodrošina visu mikobaktēriju šūnu augšanu. Šajā sakarībā, lai uzlabotu veiktspēju, ieteicams vienlaicīgi izmantot 2-3 dažādu sastāvu uzturvielas.
PVO iesaka Lowenstein-Jensen barotni kā standarta tuberkulozes izraisītāja primārās izolācijas līdzekli un tā jutīguma noteikšanu. Tā ir blīva olu barotne, kurā mikobaktēriju augšanu iegūst 20.-25. Dienā pēc bakterioloģiski pozitīva materiāla sēšanas. Bakterioskopiski negatīva materiāla kultūrām nepieciešams ilgāks inkubācijas periods (līdz 10-12 nedēļām).
Mūsu valstī piedāvātais E.R. Finn Egg Medium Finn II. Tas atšķiras ar to, ka L-asparagīna vietā tā izmanto mononātrija glutamātu, kas izraisa citus mikobaktēriju aminoskābju sintēzes veidus. Pieaugums šajā vidē ir nedaudz agrāk, un mikobaktēriju sekrēcijas biežums ir par 6–8% lielāks nekā Levenshtein-Jensen vidē.
Lai uzlabotu ekstrapulmonālās tuberkulozes bakterioloģiskās diagnozes efektivitāti, ieteicams iekļaut Finn-II modificēto mediju barības vielu kompleksā. Lai paātrinātu augšanu, uzturvielas vidē Finn-II pievieno nātrija tioglikolātu (0,05%), kas samazina skābekļa koncentrāciju. Lai aizsargātu mikobaktēriju fermentu sistēmas no toksiskiem lipīdu peroksidācijas produktiem, α-tokoferola acetāta antioksidants tiek ievadīts barotnes vidē Finn-II ar koncentrāciju 0,001 µg / ml. Sēšanas diagnostikas materiāls, kas iegūts, izmantojot standarta metodi.
Krievijas antitubulārajās laboratorijās tiek izmantotas citas blīvas barības vielu izmaiņas; G.G. Mordovijas barības vielu barotne "New", izstrādāta V.A. Anikin barības vielu barotne A-6 un A-9 utt.
Sakarā ar to, ka ķīmijterapijas laikā ir bojātas dažādas mikrobu šūnu vielmaiņas sistēmas, daļa mikobaktēriju populācijas zaudē spēju normāli attīstīties parastās barības vielās un prasa osmotiski līdzsvarotu (daļēji šķidru vai šķidru) barības vielu barotni.
Sēšanas diagnostikas materiāla rezultātu novērtēšana un reģistrēšana
Daži celmi un mikobaktēriju veidi aug lēni, augšana var parādīties pat 90. dienā. Šādu kultūraugu skaits ir neliels, bet tas iztur tos no termostata kultūrām 2,5-3 mēnešus.
Mycobacterium tuberculosis virulentās kultūras parasti aug uz blīviem olu barotnēm, veidojot dažādu izmēru un sugu R-veida kolonijas. Kolonijas ir sausas, grumbušas, ziloņkaula, nedaudz pigmentētas. Citās vidēs Mycobacterium tuberculosis kolonijas var būt mitrākas. Pēc ķīmijterapijas kursa vai ārstēšanas gaitā var atbrīvoties gludas kolonijas ar mitru augšanu (S-formas).
Izolējot kultūras, tiek izmantots speciālu pētījumu komplekss, kas ļauj atšķirt mikobaktēriju tuberkulozi no mikrobaktērijām un skābju rezistentiem saprofītiem.
Pozitīva atbilde tiek sniegta pēc obligātas mikroskopiskas Zil-Nelsen krāsotas uztriepes pārbaudes no audzētām kolonijām. Mikobaktēriju augšanas gadījumā uztriepēs ir spilgti sarkani stieņi, kas atrodas atsevišķi vai grupās, veidojot kopas filca vai bizītes veidā. Jaunajās kultūrās, kas īpaši izolētas no ilgstoši ārstētiem pacientiem ar ķīmijterapiju, mikobaktērijām ir raksturīgs izteikts polimorfisms līdz īsu, gandrīz kokcoidu vai garu variantu klātbūtnei, līdzīgi sēņu micēlijam, kopā ar stieņu formām.
Mikobaktēriju augšanas ātrumu norāda ar šādu shēmu: (+) - 1-20 CFU testa mēģenē (maza baktēriju izdalīšanās); (++) - 20-100 CFU in vitro (vidēja baktēriju izdalīšanās); (+++) -\u003e 100 CFU in vitro (bagātīga baktēriju ekskrēcija). Tuberkulozes laboratorijas diagnostikā nepietiek, lai sniegtu atbildi, vai mikobaktēriju konstatē ar šo vai šo metodi. detalizēti izprast mikobaktēriju populācijas apjomu un raksturu, tā sastāvu un īpašības. Šie dati ļauj pareizi interpretēt procesa stāvokli, plānot taktiku un nekavējoties izlabot ārstēšanu.
Pēdējos gados, lai paātrinātu mikobaktēriju augšanu, ir ierosināti barības vielas uz agara bāzes ar dažādiem augšanas piedevām un īpašu gāzu maisījumu. Lai panāktu mikobaktēriju augšanu šajās barotnēs audzēšanas laikā, izveidojiet atmosfēru ar augstu oglekļa dioksīda saturu (4-7%). Šim nolūkam tiek izmantoti īpaši CO 2 inkubatori. Tomēr vispopulārākās automatizētās mikobaktēriju audzēšanas: MGIT-BACTEC-960 un MB / Bact.
Viena šāda sistēma ir MGIT sistēma (mikobaktēriju augšanas indikācijas caurule), kas ir augsto tehnoloģiju attīstība, kas paredzēta, lai paātrinātu tuberkulozes bakterioloģisko diagnozi un noteiktu mikobaktēriju jutību pret pirmās līnijas zālēm un dažām otrās līnijas zālēm. MGIT ir vērsta uz to, lai to izmantotu kā daļu no VASTES-960 ierīces. Mikroorganismus kultivē īpašās caurulēs ar šķidru barotni, pamatojoties uz modificētu vidēju Middlebrook-7H9. Lai stimulētu mikobaktēriju augšanu un kavētu svešu mikrofloru, MGIT augšanas papildinājumu un antibakteriālo zāļu PANTA maisījumu.
Mikroorganismu augšanas reģistrācija notiek optiski. Tas balstās uz fluorescenci, ko izraisa skābekļa patēriņš mikobaktēriju augšanas procesā. Ar skābekli atkarīga fluorohroma krāsviela atrodas īpašas mēģenes apakšā un ir pārklāta ar silikona slāni. Mikobaktēriju vairošanās izraisa skābekļa daudzuma samazināšanos mēģenē un tā koncentrācijas samazināšanos, kas izraisa fluorescences palielināšanos, kas kļūst redzama, kad caurule ir apstarota ar ultravioleto gaismu un automātiski tiek konstatēta ar VASTES-960 ierīcē iebūvētajiem foto sensoriem. Spīduma intensitāte tiek reģistrēta augšanas vienībās (GU-augšanas vienības). Augšanas dati tiek ievadīti datorā, kur to var automātiski saglabāt. Augšanas līkņu datoranalīze var sniegt informāciju par dažādu mikobaktēriju pūlu klātbūtni, ieskaitot ne-tuberkulozus, kā arī palīdz novērtēt mikobaktēriju augšanas īpašības.
Šādu sistēmu ieviešanas rezultātā tika ievērojami samazināts mikobaktēriju augšanas laiks, vidēji 11 dienas WASTES-960 un 19 dienas MB / Bact un 33 dienas standarta blīvā barotnē. Jāatzīmē, ka šīm sistēmām ir vajadzīgs augsti kvalificēts personāls. Sēšanas materiāls uz šķidrajiem medijiem jāpapildina ar sēšanu uz Levenshteyn-Jensen barotnes, kurai ir svarīga loma, ja tuberkuloze neizraisa augšanu citos medijos.
Mikobaktēriju zāļu jutības noteikšana
Mikobaktēriju spektra un jutības pakāpes noteikšanai pret tuberkulozes zālēm ir nozīmīga klīniskā nozīme, kā arī zāļu rezistentās tuberkulozes izplatības epidemioloģiskais novērtējums. Turklāt zāļu rezistences uzraudzība ļauj novērtēt visas pret tuberkulozes programmas efektivitāti, jo tas ir neatņemams visu tuberkulozes apkarošanas darbību komponentu darba rādītājs.
Zāļu jutīguma daudzveidība un laiks:
- pirms ārstēšanas uzsākšanas, lai noteiktu ārstēšanas stratēģiju un taktiku:
- izolējot no pacientu kultūrām no dažādiem materiāliem (krēpām, BAL, urīnu, eksudātiem, šķidrumiem utt.), pārbauda visus izolētos celmus:
- intensīvas terapijas fāzes beigās, ja nav klīniskās un radioloģiskās dinamikas:
- ja nepieciešams, mainiet ārstēšanas shēmu, ja:
- krēpu negatīvisma trūkums;
- kultūras atkārtota izolēšana pēc krēpu negatīvisma;
- straujš KUM skaita pieaugums uztriepēs pēc sākotnējā samazinājuma. Ir labi zināms, ka Mycobacterium tuberculosis celmi, kas ir neviendabīgi attiecībā uz zāļu jutīgumu, tiek izolēti no materiāla, ko iegūst no tuberkulozes pacienta. Celmu jutīgums pret zālēm pret tuberkulozi var atšķirties atkarībā no zāļu klāsta, pretestības pakāpes, biežuma un ātruma.
Mycobacterium tuberculosis zāļu rezistences pakāpe tiek noteikta saskaņā ar noteiktajiem kritērijiem, kas ir vērsti uz rezistences klīnisko nozīmību un ir atkarīgi no zāļu pret tuberkulozes aktivitātes, tā farmakokinētikas un koncentrācijas bojājumā. maksimālā terapeitiskā deva un tā tālāk.
Mikobaktēriju jutības noteikšana šobrīd tiek veikta ar mikrobioloģiskām metodēm:
- absolūtās koncentrācijas (atšķaidīšanas metode uz cietas vai šķidras barības vielas), \\ t
- proporcijas
- pretestības koeficients.
Rezistence parasti izpaužas kā vizuāli novērota Mycobacterium tuberculosis koloniju augšana, tomēr ir metodes, kas izraisa Mycobacterium šūnu dalīšanās sākumposmā krāsu reakciju veidā. Šīs metodes samazina testa laiku no 3-4 nedēļām.
PVO ķīmijterapijas komitejas ieteiktā absolūtās koncentrācijas metode, kas no metodoloģiskā viedokļa ir visvienkāršākā, bet prasa augstu standartizāciju un laboratorijas procedūru precizitāti, ir kļuvusi plaši izplatīta Krievijā. Zāļu jutības tests sastāv no cauruļu kopas ar barības vielu barotni, kas modificēta ar pret tuberkulozes zālēm. Komplekts sastāv no 2-3 caurulēm ar dažādām koncentrācijām katrā no izmantotajām zālēm, vienu kontroles cauruli ar barotni bez medikamenta un vienu cauruli, kas satur 1000 μg / ml nātrija salicilāta vai 500 μg / ml para-nitrobenzoskābes, lai noteiktu ne-tuberkulozas mikobaktēriju augšanu.
Lai sagatavotu mediju komplektu ar zālēm, izmantojot modificētu vidēju Lowenstein-Jensen (bez cietes), kas ielej kolbās. Katrā kolbā pievieno noteiktu daudzumu atbilstošas atšķaidīšanas pret TB. Kolbu saturu rūpīgi samaisa, ielej testa mēģenēs un 40 minūtes slīpā stāvoklī velmē 85 ° C temperatūrā. Ieteicams saudzēt barotni elektriskā skrūvgriezī ar automātisku temperatūras kontroli. Vidēja viela ar pret tuberkulozi
1. rindu var uzglabāt ledusskapī 2–4 ° C temperatūrā 1 mēnesi, ar otrās rindas narkotikām - ne vairāk kā 2 nedēļas. Nav pieņemams uzglabāšanas līdzeklis ar zālēm istabas temperatūrā. Sagatavojot anti-tuberkulozes medikamentu risinājumus, tiek ņemta vērā to aktivitāte, aprēķinot koncentrāciju, kas koriģēta atbilstoši nespecifiskās zāļu daļas tīrībai, tīrībai utt. Noteikt zāļu jutīgumu, izmantojot tikai ķīmiski tīras vielas.
Metodes princips ir noteikt anti-tuberkulozes zāļu koncentrāciju, kas nomāc ievērojamu mikobaktēriju populācijas pieaugumu. Pareizi izpildot šo metodi, ir laba precizitāte.
Pirms testēšanas nepieciešams pārliecināties, ka izvēlētajai Mycobacterium tuberculosis kultūrai nav svešas mikrofloras. No mikobaktēriju kultūras 0,9% nātrija hlorīda šķīdumā tiek sagatavota viendabīga suspensija, kas satur 500 miljonus mikrobu šūnu 1 ml (optiskās duļķainības standarts 5 vienības). Iegūto suspensiju atšķaida ar 0,9% nātrija hlorīda šķīdumu (1:10) un 0,2 ml suspensijas pievieno katrai kultūras barotnes mēģenei. Uzklātās caurules ievieto termostatā 37 ° C temperatūrā un 2-3 dienas tur horizontālā stāvoklī, lai barotnes vidēja slīpā virsma tiktu vienmērīgi inokulēta ar mycobacterium tuberculosis suspensiju. Tad caurules pārnes vertikālā stāvoklī un inkubē 3-4 nedēļas. Rezultātu mērīšana notiek 3-4 nedēļās.
Tā kā patogēna izolācijas laiks no klīniskā materiāla uz barības vielām ir vismaz 1–1,5 mēneši, narkotiku jutības noteikšanas rezultātus ar šo metodi var iegūt ne agrāk kā 2–2,5 mēnešus pēc materiāla sēšanas. Tas ir viens no galvenajiem metodes trūkumiem.
Interpretēt mikobaktēriju jutīguma noteikšanas rezultātus, pamatojoties uz noteiktiem kritērijiem. Blīvā vidē tiek uzskatīts, ka kultūra ir jutīga pret medikamenta koncentrāciju, ja šajā mēģenē audzēto mikobaktēriju koloniju skaits ar šo medikamentu nepārsniedz 20 ar plašu augšanu uz kontroles caurules bez zālēm. Tikai vairāk nekā 20 koloniju klātbūtnē kultūra tiek uzskatīta par rezistentu pret šo koncentrāciju. Praksē, saņemot eksperimentālo cauruļu izaugsmes rezultātus, gandrīz 20 CFU. ir jāinformē klīniskā vienība, ka šajā gadījumā jutīgums vai stabilitāte ir robežas, jo tas dažreiz var izskaidrot klīnisko rādītāju neskaidru dinamiku.
Dažādām zālēm tiek noteikta noteikta koncentrācija, kurā tiek novērota kritiskās mikobaktēriju populācijas vairošanās. Šīs koncentrācijas sauc par "kritiskām". Kā stabilitātes kritērijs tiek izmantots mikobaktēriju populācijas augšanas ātrums barības vidē ar narkotiku kritiskā koncentrācijā.
Iekšējā ftisioloģiskajā praksē zāļu rezistences noteikšana neaprobežojas tikai ar kritisko koncentrāciju noteikšanu. Tas ir saistīts ar faktu. ka patogēno zāļu rezistences līmeņa paplašināta noteikšana ļauj ārstam precīzāk veidot ķīmijterapijas taktiku, izmantojot zināšanas par zāļu kombināciju pastiprinošo iedarbību, paredzēt krustenisko rezistenci, vai izmantot efektīvākas zāles, ko lieto pret tuberkulozi lietoto zāļu grupas.
Absolūtā koncentrācijas metode ir visvienkāršākā, bet arī visjutīgākā pret kļūdām, kas veiktas, veicot to. Uzticamāka, jo īpaši, nosakot jutību pret otrās līnijas zālēm, un proporciju metode ir izplatīta ārpus Krievijas. Tajā ir ņemtas vērā absolūtās koncentrācijas metodes nepilnības, taču tas ir vairāk laika.
Metode ir ļoti līdzīga absolūtās koncentrācijas metodei. Testa mēģenes sagatavošana ar tādiem pašiem veidiem. kā absolūtā koncentrācijas metode. Tomēr Mycobacterium tuberculosis suspensijas sējas devu samazina par 10 reizēm. tas nosaka dažu Mycobacterium tuberculosis celmu spontānās rezistences biežumu pret zālēm, piemēram, etambutolu, protionamīdu, kapreomicīnu. Kā kontroli, izmantojiet 2 vai 3 caurules ar sēklu devu, kas ir vienāda ar testa mēģenēm, sērijveidā atšķaidot 10 un 100 reizes. Izturības kritērijs ir vizuāli novērotā Mycobacterium tuberculosis augšanas proporcija. Pirmajā rindā esošajiem medikamentiem ilgtspējības kritērijs ir pieaugums par 1% no sākotnējās populācijas, otrās rindas narkotikām - pieaugums 1 vai vairāk nekā 10% no sākotnējās, atkarībā no izvēlētās kritiskās koncentrācijas.
1997. gadā PVO un Starptautiskās pret tuberkulozes apkarošanas savienības darba grupa, lai atklātu pret tuberkulozi vērstu zāļu rezistenci, pielāgoja šos kritērijus, norādot, ka mikobaktērijas, kas aug uz Levenshteyn-Jensen blīvā olu barotnē, uzskatāmas par stabilām šādās koncentrācijās:
- dihidrostreptomicīns - 4 µg / ml;
- izoniazīds - 0,2 µg / ml:
- rifampicīns - 40 µg / ml:
- Etambutols - 2 µg / ml.
2001. gadā tika ierosinātas kritiskās koncentrācijas šādām otrās līnijas zālēm (kritiskā daļa - 1%):
- kapreomicīns - 40 µg / ml;
- protionamīds - 40 µg / ml;
- kanamicīns - 30 µg / ml;
- viomicīns - 30 µg / ml;
- cikloserīns - 40 µg / ml;
- aminosalicilskābe - 0,5 µg / ml;
- ofloksacīns - 2 µg / ml.
Izaugsmes rezultātus novērtē pēc 4 nedēļām kā provizoriskas un pēc 6 nedēļu audzēšanas gala.
Lai noteiktu narkotiku jutību pret pirazinamīdu, ko plaši izmanto modernā tuberkulozes ķīmijterapijā, ieteicamā kritiskā koncentrācija ir 200 µg / ml. Tomēr joprojām nav vispārpieņemtas metodes zāļu rezistences noteikšanai pret šo medikamentu uz cietām barotnēm, jo tās antibakteriālā aktivitāte izpaužas tikai skābā vidē (pH
Lai novērtētu mikobaktēriju jutīguma noteikšanas rezultātu kvalitāti, ieteicams katru jauno Lowenstein-Jensen barotnes partiju uzraudzīt, paralēli nosakot standarta muzejs H37Rv jutību. Turklāt ir daži mikrobioloģiskie kritēriji, kas jāizpilda, lai metodoloģija varētu radīt labi reproducējamu un pareizi interpretējamu rezultātu. Tie ietver Mycobacterium tuberculosis kultūras dzīvotspēju, noteikumus par viendabīgas suspensijas un suspensijas iegūšanu, noteikumus par Mycobacterium tuberculosis kultūru izvēli, izvēlētās baktēriju masas reprezentativitāti. Zāļu rezistences noteikšanas ticamība samazinās, ja baktēriju ekskrēcija ir ļoti vāja.
Nesen ir dota daudzsološa atzīta metode narkotiku jutīguma noteikšanai, izmantojot automatizētas sistēmas. Visprogresīvākie šajā jomā ir attīstība, kas balstīta uz WASTES MGIT-960. Šajā gadījumā mycobacterium tuberculosis narkotiku jutība tiek noteikta, pamatojoties uz modificētu proporciju metodi. Noteikšanas procesā mikobaktēriju tuberkulozes augšanas ātrums tiek salīdzināts kontroles caurulē un testa mēģenēs ar zālēm. SIRE komplektā iekļautie bagātinātāji un antibiotikas tiek lietotas, lai noteiktu jutību pret streptomicīnu, izoniazīdu, rifa pikīnu un etambutolu. Lai noteiktu jutību pret pirazinamīdu, izmantojiet PZA komplektu. Testa laikā mikobaktēriju tuberkulozes suspensiju inokulē ar mēģenēm ar zālēm, kā arī kontroles caurulēm ar 100% atšķaidīšanu visiem preparātiem, izņemot pirazinamīdu, kur suspensijas atšķaidījums ir 10 reizes. Ilgtspējas kritērijs ir mikobaktēriju pieauguma rādītājs 100 GU, kad tiek sasniegts kontroles kontroles mēģenes 400 GU pieaugums (sk. „Mikobaktēriju izolācijas kultūras metodes”). Rezultātu uzskaite un interpretācija tiek veikta automātiski, un to nosaka ievadītā vai atlasītā programma.
Kā kritiskās koncentrācijas galīgās koncentrācijas tiek izmantotas mēģenē ar šķidru barības vielu. Pašlaik kritiskās koncentrācijas ir izstrādātas gan 1. rindas zālēm, gan dažām 2. rindas zālēm. Jāatzīmē, ka Mycobacterium tuberculosis jutības noteikšana pret cikloserīnu un aminosalicilskābi tiek veikta tikai uz olu barības vielām.
Sīki izstrādāts darba protokols, izmantojot aprakstīto sistēmu, ļauj veikt pētījumu par zāļu jutību gan izolētajā kultūrā (ar blīvu barības vielu), gan izmantojot mikobaktēriju primāro augšanu MGIT mēģenē. Pēdējā iespēja ievērojami samazina kultūras pētījumu laiku, ļaujot jums iegūt pilnīgus rezultātus par Mycobacterium tuberculosis kultūru (ieskaitot informāciju par zāļu jutību) pēc 3 nedēļām no materiāla savākšanas dienas, bet tradicionālo metodi var iegūt tikai līdz 3. mēnesim. Iegūtais laiks, kad pacients atrodas intensīvajā ārstēšanas fāzē, var kompensēt relatīvās augstās pētniecības izmaksas.
Mikobaktēriju diferenciācija
Ņemot vērā to, ka izmantotie barības vielu nesēji nav stingri selektīvi. turpmāka izolēto mikobaktēriju diferenciācija tiek atzīta par obligātu. Mikobaktēriju diferenciācijas nepieciešamība ir saistīta ar vairākām ģints ģenētisko procesu izraisīto patoloģisko procesu pazīmēm: atšķirīgs tuberkulozes un mikobaktēriju gaita un iznākums, dabiska zāļu rezistence pret dažām pret tuberkulozes zālēm.
Ir atzīts, ka M. tuberculosis kompleksa mikobaktēriju primārā identifikācija no ne-tuberkulozes mikobaktērijām tiek veikta saskaņā ar šādām īpašībām: augšanas ātrums uz blīvu barības vielu barotnēm, pigmentācija, kolonijas morfoloģija, skābju rezistences klātbūtne un augšanas temperatūras optimums.
Diemžēl nav nevienas laboratorijas metodes, kas varētu droši atšķirt M. tuberculosis kompleksa mikobaktērijas no citiem skābju rezistentiem mikobaktērijiem, tomēr iepriekš minēto pazīmju kombinācija ar vairāku turpmāk uzskaitīto bioķīmisko testu rezultātiem ļauj identificēt M. tuberculosis kompleksa mikobaktērijas ar varbūtību 95%.
Lai diferencētu M. tuberculosis kompleksa (M. tuberculosis, M. bovis, M. bovisBCG, M. africanum, M. microti, M. canettii uc) mikobaktērijas no lēni augošas ne-tuberkulozes mikobaktērijām, tiek izmantoti pamata bioķīmiskie testi, lai noteiktu šādas pazīmes:
- spēja ražot nikotīnskābi (niacīna tests):
- nitrāta reduktāzes aktivitāte;
- termostabilā katalāze;
- augšanu uz barotnes ar nātrija salicilātu (1 mg / ml).
Kā papildus jūs varat izmantot arī augšanas testus uz barotnes, kas satur 500 μg / ml p-nitrobenzoskābes vai 5% nātrija hlorīda.
Daudzas bakterioloģiskās laboratorijas šos mikroorganismus identificē tikai kompleksa līmenī, kas ir saistīts ar laboratoriju ierobežotajām iespējām un speciālistu metodiskajām iespējām.
Vairumā gadījumu M. tuberculosis un M. bovis diferencēšanai praksē pietiek ar šādiem testiem: niacīns, nitrātu reduktāzes klātbūtnei, pirazinamidāzes klātbūtnei un augšanas reģistrācijai barotnē, kas satur 2 μg / ml tiofēn-2-karbonskābes hidrazīda. Tajā pašā laikā tiek ņemts vērā, ka M. tuberculosis kompleksa mikobaktērijas raksturo šādas īpašības:
- lēna izaugsme (vairāk nekā 3 nedēļas);
- augšanas temperatūra no 35 līdz 37 o C;
- pigmenta veidošanās trūkums (ziloņkaula krāsa);
- izteikta skābes izturīga krāsa;
- pozitīva niacīna mīkla;
- pozitīvs nitrāta reduktāzes tests;
- termostabilas katalāzes trūkums (68 ° C).
- izaugsmes trūkums vidē Lowenstein-Jensen, kas satur: \\ t
- 1000 µg / ml nātrija salicilāta, \\ t
- 500 µg / ml paranitrobenzoskābes, \\ t
- 5% nātrija hlorīds:
- augšana 1–5 μg / ml tiofēn-2-karbonskābes klātbūtnē.
Izolēto mikobaktēriju diferenciācijas nozīmīgums ievērojami palielināsies, palielinoties ar tuberkulozi vai mikobaktēriju saistītu HIV / AIDS gadījumu reģistrācijas biežumam. Pašlaik nav absolūtas pārliecības par to, ka praktiskās reģionālās laboratorijas ir gatavas pareizi veikt šo darbu.
Tuberkulozes imunoloģiskā diagnoze
Ir vairākas universālas parādības, narkotikas un imunoloģiskie testi, kas sākotnēji tika atklāti tuberkulozes laikā vai imūnās atbildes reakcijas uz mikobaktērijām modeli. Tie ir BCG un tuberkulīns, fenomens, piemēram, ādas HRT (tuberkulīna testi - Pirke un Mantoux reakcijas), reakcija uz tuberkulīna subkutānu ievadīšanu jutīgiem dzīvniekiem (Koch fenomens). Dažas no pirmajām infekcijas slimības antivielām tika konstatētas arī tuberkulozē. Protams, jo dziļāka izpratne par imunitātes pret tuberkulozi mehānismiem un to ģenētisko kontroli, jo plašāka var būt imunoloģisko metožu un medikamentu izmantošana, kas ietekmē imūnsistēmu, lai atrisinātu praktiskās problēmas, kas saistītas ar fthisiology.
Pašlaik svarīgākā un sarežģītākā praktiskā problēma tiek uzskatīta par tuberkulozes atklāšanu iedzīvotāju masu skrīninga procesā. Tomēr, neskatoties uz daudziem ziņojumiem par „panākumiem” (par ierobežotu materiālu), nav piemērotas imunoloģiskās metodes (atveidotas „jebkurās rokās”) un preparāts šiem mērķiem.
Klīniskajā praksē ļoti plaši tiek izmantotas imunoloģiskās metodes, jo īpaši seroloģiskie pētījumi (antigēnu, antivielu noteikšana) un tuberkulīna provokācijas testi.
Pirmkārt, starp imunoloģiskajiem pētījumiem, ko izmanto diferenciāldiagnozē, ir seroloģiskās metodes - antigēnu un antivielu definīcija dažādos ķermeņa materiālos.
Mycobacterium tuberculosis antivielu noteikšanas specifika ir atkarīga no imūnanalīzē izmantotajiem antigēniem. Ir ierosināts ievērojams antigēnu daudzums, no kuriem pirmais ir tuberkulīna PPD:
- PPD un citi kompleksie preparāti no kultūras šķidruma;
- ultraskaņas noārdīšanās;
- tritona ekstrakts un citi kompleksie šūnu sienu preparāti;
- 5 antigēns (Daniel);
- 60 antigēns (Coccito);
- lipoarabinomannāns;
- vadu faktors (trehalozes-6,6-diolāts);
- fenola un citi glikolipīdi;
- lipopolizaharīdi;
- fibronektīna saistošu antigēnu;
- olbaltumvielas (visbiežāk rekombinants); 81,65,38,34,30,19,18,16,15,12 KDA un citi.
Krievu un ārvalstu zinātnieku pētījumu rezultātā tika atklāti galvenie antivielu ražošanas modeļi un tuberkulozes seroloģiskās diagnozes efektivitāte: jo sarežģītāks ir antigēns, jo augstāks jutīgums un mazāks testu specifiskums. Specifiskums. \\ T dažādās valstīs atšķiras atkarībā no M. tuberculosis populācijas infekcijas un ne-tuberkulozes mikobaktērijām, BCG vakcinācijas utt. Bērniem serodiagnozes informācijas saturs ir mazāks nekā pieaugušajiem. Primārajā tuberkulozē (bieži bērni) IgM definīcija ir informatīvāka. ar sekundāro - IgG. HIV inficētajā serodiagnostikas informācijā antivielu noteikšana samazinās. Antivielu noteikšanas efektivitāte ir atkarīga no vairākiem „klīniskiem momentiem”: procesa aktivitāte (mikobaktēriju “izolācijas” klātbūtne vai neesamība, sabrukšanas dobumu klātbūtne, infiltrācijas pakāpe), procesa izplatība, tās ilgums.
Enzīmu imūnanalīzes (ELISA) metodes jutība ir aptuveni 70%. Pētījuma efektivitātes trūkums ir saistīts ar tā zemo specifiku. Iepriekš tika apsvērta iespēja izmantot seroloģisko skrīningu grupās augsts risksjo īpaši tiem, kam pēc tuberkulozes ir plaušu pārmaiņas.
Lai palielinātu ELISA specifiku, turpina meklēt specifiskākus antigēnus, tostarp tos, kas iegūti gēnu inženierijā, ESAT-6 un citi (skatīt iepriekš). Stingri specifisku antigēnu (38 kDa, ESAT) lietošana palielina specifiskumu. bet ievērojami samazina analīzes jutīgumu. Papildus ELISA (eksperimentālās laboratorijas testu sistēmas, piemēram, Pathozyme ELISA komplekts) tika piedāvātas arī imūnochromatogrāfijas komplekti ar sānu filtrāciju (Mycodot), kā arī citi līdzīgi testi (punktu analīze uz membrānas) ar vizuālu testa rezultātu. Veicot šos testus, analīze notiek 10-30 minūšu laikā; tām nav nepieciešama īpaša iekārta, ir nepieciešams vizuāls rezultātu novērtējums, kas saistīts ar zināmu subjektīvību. Šīm metodēm ir aptuveni tādas pašas jutības un specifiskuma pazīmes (attiecīgi 70% un 90-93%) kā tradicionālā ELISA.
Imūnanalīzes metožu izmantošanai ir zināma vērtība kā papildu metode, kas tiek ņemta vērā izmantoto metožu kompleksā tuberkulozes diferenciāldiagnozē, īpaši tās ekstrapulmonālo formu diagnostikā. ELISA ir visefektīvākā tuberkuloza meningīta diagnosticēšanai cerebrospinālā šķidruma pētījumā. Šajā gadījumā analīzes jutīgums ir 80-85%, un specifiskums ir 97-98%. Ir pierādījumi par to, ka tuberkulozes uveīta diagnosticēšanā asins šķidrumā tiek konstatētas antivielas pret mikobaktēriju tuberkulozi.
Gamma-interferona sintēzes indukcija in vitro
Gamma-interferons (IFN-γ) ir specifiskas imūnās aizsardzības faktors, kas tiek realizēts, aktivizējot makrofāgu fermentu sistēmas. IFN-γ sintēzes izraisīšana ar sensibilizētiem T-limfocītiem izraisa to mijiedarbību ar mikobaktēriju antigēniem.
Kā antigēni izmanto kā tuberkulīna PPD. un specifiskie antigēni, kas iegūti, izmantojot gēnu inženieriju, jo īpaši antigēni ESAT-6 (agri izdalīts antigēns ar molekulmasu 6 kDa) un CFP-10 (proteīna kultūras filtrāts, 10 kDa). BCG vakcīnas un citu mikobaktēriju šūnās nav ģenētiskās inženierijas vai rekombinanto antigēnu. Izmantojot tuberkulīnu, IFN-γ indukcijas testa rezultāti ir salīdzināmi ar tuberkulīna ādas testa rezultātiem (tieša korelācija). Lietojot ģenētiski modificētus antigēnus, testa rezultāti ir specifiskāki un nav atkarīgi no iepriekšējās BCG vakcinācijas. Pārbaudot vakcinētos cilvēkus, kuriem nebija kontakta ar tuberkulozes infekciju, testa specifika ir 99%. Testa jutīgums pacientiem ar tuberkulozi svārstās no 81 līdz 89%.
Ir izstrādāti testu un diagnostikas testi, kas balstīti uz asins šūnu vai mononukleāro šūnu, kas izolētas no asinīm, īslaicīgu kultivēšanu ar in vitro Mycobacterium tuberculosis antigēniem, pēc tam nosakot IFN-γ koncentrāciju vai aprēķinot IFN-y sintezējošo T-limfocītu skaitu. In vitro sintezētā interferona koncentrācija, ko nosaka ar ELISA palīdzību, izmantojot monoklonālas antivielas, kas saistās ar IFN-γ. Pēc tam, izmantojot kalibrēšanas standartu, IFN-γ nosaka tā koncentrāciju testa mēģenē vai tabletes iedobēs.
Veicot Elispot testu, T-limfocītu skaits, kas sintezē IFN-γ. uz kausa virsmas, pārklāts ar antivielām pret IFN-γ.
diagnostikas izstrādātāji, kas balstīti uz IFN-γ indukciju in vitro, ko apstiprinājusi ASV Narkotiku un zāļu aģentūra, apgalvo, ka ar testa palīdzību nav iespējams diferencēt latento tuberkulozes infekciju no aktīvas tuberkulozes. Tāpēc reģionos ar augstu infekcijas līmeni testam nav tiešas diagnostikas vērtības. Tomēr mūsu valstī to var izmantot, lai diferencētu tuberkulozes infekcijas bērniem pēc vakcinācijas ar alerģijām, kā arī novērtētu specifiskās imunitātes līmeni ārstēšanas procesā.
Pašlaik tiek pētīta vietējā testēšanas sistēma, lai noteiktu specifisku tuberkulozes antigēnu IFN-γ sintēzes indukciju in vitro.
Imūnsistēma un tuberkulozes gaita, imunokorekcija
Cilvēku tuberkulozes ārstēšanas procesā notiek izmaiņas antigenēmijā un imūnsistēmas stāvoklī.
Dati par eksudātu un audu izmaiņām ir lielā mērā pretrunīgi. Vienīgais, ko var atzīmēt ar pilnīgu pamatojumu, ir tas, ka ievērojams skaits aktivēto T-limfocītu parasti atrodami tuberkulārās granulomos.
Ir jēga turpināt vēl divus punktus, kas ir nepieciešami, lai saprastu imunoloģisko mehānismu nozīmi tuberkulozes ārstēšanā cilvēkiem:
- pacientiem ar AIDS ir īpaši liela rezistence pret vairāku zāļu lietošanu;
- vairāku zāļu rezistences gadījumā (un, ja nav HIV infekcijas), imunitātes traucējumi (pirmkārt, T-šūnu komponents) ir īpaši nozīmīgi.
Tuberkulozē plaši tiek pielietotas dažādas imunokorekcijas metodes: tās galvenokārt ir zāles, kas galvenokārt darbojas T-šūnu imunitātei un mononukleāro fagocītu sistēmai (aizkrūts hormoni, izofons, licopīds, poloksidonijs uc). kā arī veselas (novājinātas) mikobaktērijas un to sastāvdaļas.
Tuberkulozes molekulārā bioloģiskā diagnostika
Molekulārās bioloģijas metodes infekcijas slimību diagnosticēšanā galvenokārt ietver metodes, kas balstītas uz baktēriju un vīrusu patogēnu manipulācijām ar genomiskiem materiāliem, lai noteiktu specifiskus ģenētiskos materiālus - DNS segmentus ar specifisku šīs sugas vai patogēnu celmu specifiku. DNS sekvences gēnos, kas nosaka patogēna jutību pret noteiktām zāļu vielām, kā arī analizē šo funkciju dažu patogēnu gēnu linu aktivitāte. Molekulārās bioloģiskās metodes plaši izmanto zinātniskajos pētījumos un praktiskā pielietojumā dažādu baktēriju un vīrusu infekciju diagnosticēšanā un kontrolē pēc tam, kad 1985. gadā atklāja Kerry Mulllis (1989. gada Nobela prēmijas laureāts) par polimerāzes ķēdes reakciju.
Polimerāzes ķēdes reakcijas metodes principi un iespējas
PCR ļauj jums in vitro vairot (vairoties) nukleotīdu secību (patogēnu DNS fragmentu) vairākas stundas miljonu reižu laikā. Reakcijas vadīšana atsevišķu DNS virzienu klātbūtnē nosaka analīzes ārkārtīgi augsto jutību.
Dažu DNS ķēdes posmu nukleotīdu secība nosaka mikroorganisma ģenētisko identitāti, kas izskaidro PCR augsto specifiku.
Šīs metodes vērtība mikobaktēriju tuberkulozes īpašību noteikšanai un izpētei ir saistīta ar bioloģiskās īpašības mikroorganisms ar ļoti lēnu augšanu: Mycobacterium tuberculosis DNS divkāršošanās laiks audzēšanas laikā ir 12-24 stundas.
PCR metodes princips ir pastiprināšana - vairāki, miljoniem reižu. specifiskas DNS sekvences sekciju pavairošana mēģenē mikrovolumā ar sekojošu trīs reakcijas posmu ciklisku atkārtošanos, katrs no tiem notiek citā temperatūras režīmā:
- I posms - divslāņu DNS denaturācija, sakarsējot ar tās ķēdes novirzi;
- II posms - primeru (primer oligonukleotīdu) komplementārā saistīšanās (hibridizācija) līdz stingri specifisko ķēžu gala sekcijām, kas izvēlētas DNS fragmenta vairošanai;
- III posms - DNS fragmenta ķēdes pabeigšana, izmantojot termostabilu DNS polimerāzi.
Lai pastiprinātu in vitro, jābūt veidnes DNS molekulām. četri dezoksinukleozīdu trifosfātu (nukleotīdu) veidi, kas satur atbilstošas slāpekļa bāzes: adenīns (A), timīns (T), guanīns (D), citozīns (C); mākslīgi sintezēti sēklu oligonukleotīdi (primeri), kas sastāv no 18-20 bāzes pāriem; termostabils DNS polimerāzes enzīms, kura temperatūras optimums ir 68-72 o C un magnija joni.
PCR specifika ir atkarīga no DNS fragmenta izvēles. Saskaņā ar to sintēze sānu sēklu oligonukleotīdi. Hibridizācijas specifiku un DNS ķēdes pabeigšanu nosaka ar šādu slāpekļa bāzu pāru komplementaritātes principu: adenīna-timīns, guanīna-citozīns.
Lai noteiktu mikobaktēriju tuberkulozes kompleksa genomu, vairumā testa sistēmu visefektīvākais amplifikācijas mērķis ir DNS fragments IS6110, kas lielākajā daļā mikobaktēriju tuberkulozes celmu ir ievērojams skaits (10-20) atkārtojumu genomā, kas kopā ar specifiskumu nodrošina augstu analīzes jutību. Tajā pašā laikā ir aprakstīti Mycobacterium tuberculosis celmi ar nelielu atkārtojumu skaitu vai IS6110 fragmenta neesamību.
DNS molekulu izolēšana no bioloģiskā parauga
PCR gadījumā ierosinātāja DNS ir jāizolē no bioloģiskā materiāla minimālā daudzumā, minimālais daudzums neeksistējošas DNS un dažādi fermentu inhibitori - DNS polimerāze.
Paraugu sagatavošana jāveic apstākļos, kas novērš pētāmo paraugu savstarpēju inficēšanos ar izdalītajām DNS molekulām. Tas prasa telpas iepriekšēju apstrādi ar ultravioleto gaismu, grīdām un galdu un ierīču darba virsmām - hloru saturošiem šķīdumiem. Tāpat ir nepieciešams izmantot tīrus cimdus, vienreizējās lietošanas mēģenes un padomus automātiskām pipetēm.
Lai izolētu Mycobacterium tuberculosis DNS no klīniskajiem paraugiem (cerebrospinālais šķidrums, bronhiālā skalošana), kas nesatur lielu skaitu leikocītu, šūnu atliekas vai sāļus, pietiek ar parauga centrifugēšanu 3-4 tūkstoši apgriezienu minūtē, pievienojot 20-30 μl 2% šķīduma nogulsnēm tritons X-100 un silts 30 minūtes 90 oC temperatūrā.
Krēpu paraugu pagatavošanai nepieciešama efektīva atšķaidīšana, par kuru parasti izmanto 4% nātrija hidroksīda šķīdumu un N-acetil-L-cisteīnu (NALC) 50-80 mg paraugā atkarībā no parauga viskozitātes. NALC šķīdums jāsagatavo ex tempore vai NALC pulveris var tikt pievienots sausā veidā tieši paraugam. Pēc atšķaidīšanas paraugus centrifugē 15 minūtes ar 3,5–4000 apgriezieniem minūtē (3000 g) 50 ml mēģenēs ar skrūvējamu vāciņu, t.i. tādos pašos apstākļos, kādi ieteicami pirmssēšanas sagatavošanai.
DNS ekstrakcijai no nogulumiem biežāk tiek izmantota metode, kas balstās uz 5-6 molārā guanidīna izotiocianāta šķīduma kā lizējošā reaģenta un mikroporainu silīcija daļiņu ("diatomītu zemes") sorbējošo DNS molekulu izmantošanu. Nespecifiskas vielas, ieskaitot iespējamos inhibitorus, pēc tam mazgā 2,5 molāru guanidīna izotiocianāta šķīdumā un etanola šķīdumā, pēc tam DNS molekulas tiek desorbētas ūdenī, un šos paraugus izmanto PCR. Lai vienkāršotu DNS ekstrakcijas tehnoloģiju, „diatomīta zeme” bieži tiek aizstāta ar magnētiskām mikrodaļiņām, kas pārklātas ar silīcija dioksīdu. Vienlaikus centrifugēšanas vietā tiek izmantota īpaša magnētiskā caurule mikrotesta caurulēm, lai nogulsnētu daļiņas.
Krievijā ir izstrādāta oriģināla mikobaktēriju imunomagnētiskās nošķiršanas metode, kam seko patogēna DNS ekstrakcija. Mycobacterium tuberculosis imunomagnētiskai atdalīšanai tiek izmantoti 3-5 µm ferropartikulāri, kas pārklāti ar silīcija oksīdu un kuriem poliklonālās (truša) antivielas pret tuberkulozes mikobaktērijām ir piestiprinātas ar ķīmisko savienojumu. Pēc sārmainas lizes krēpu paraugi tiek neitralizēti ar skābu Tris-HCl šķīdumu un inkubēti ar imunomagnētisko sorbentu. Tad imunopola daļiņas tiek savāktas, izmantojot magnētisko nūju ar nomaināmu uzgali, kas pārnests uz mikrovadījumu, nogulsnēts. Uzklāj 20-30 μl 2% Triton X-100 šķīdumu un 30 minūtes karsē 90 ° C temperatūrā. Supernatantu izmanto kā DNS veidni PCR analīzei.
Sarežģīta problēma ir Mycobacterium tuberculosis DNS izolācija no biopsijas paraugiem. Biopsijas lizei tiek izmantots enzīms - proteināze K gala koncentrācijā 200-500 mg / l 56 o temperatūrā. Tālāk piešķiriet vienu no zināmām metodēm. Biopsijas paraugu PCR analīzē konstatētais nespecifiskās DNS pārpalikums bieži palīdz nomākt reakciju, kas prasa atkārtotu DNS ekstrakciju.
Rezultātu noteikšanas metodes
Pēc reakcijas pabeigšanas amplificētie patogēnu DNS fragmenti tiek identificēti, izmantojot dažādas metodes.
Labi zināma gēla elektroforēzes metode. Vienlaikus iegūtais DNS fragments tiek identificēts ar pozitīvu kontroli, kas satur vēlamo specifisko DNS fragmentu, vai iepriekš zināmu fragmenta lielumu (nukleotīdu pāru skaitu), ko nosaka, izmantojot standarta molekulāro marķieri.
Konkrētas krāsvielas, etīdija bromīda klātbūtnē, kas iekļauta divslāņu DNS. Sintezētais DNS fragments tiek konstatēts kā josla, kas mirgo ultravioletā starojuma iedarbībā.
DNS fragmenta lielumam, kas noteikts ar elektroforēzi pēc attāluma no sākuma, jāatbilst zināmam molekulmasas marķierim vai pozitīvai kontrolei.
Citas metodes PCR rezultātu noteikšanai balstās uz vienas ķēdes PCR produktu hibridizāciju ar tiem pievienotu biotīnu iezīmētu DNS zondi, kam seko noteikšana ar enzīmu reakciju, piemēram, saistoties ar streptavidīna-sārmainās fosfatāzes konjugāta biotīnu.
Pamatojoties uz šāda veida noteikšanu, ir izveidoti PCR analizatori, kuros PCR rezultātu noteikšana tiek veikta automātiski, izlasot optisko blīvumu paraugos pēc fermentatīvas reakcijas.
Šo metožu trūkumi ir intralaboratoriskā piesārņojuma iespējas ar diezgan īsiem DNS molekulu fragmentiem. Šīs molekulas, izlaižot jaunizpētītajos paraugos, kļūst par PCR matricu un noved pie viltus pozitīviem rezultātiem.
Šajā sakarā, lai novērstu viltus pozitīvus rezultātus, tiek ieviesti stingri noteikumi telpu atdalīšanai un izolēšanai: DNS izolēšanai no bioloģiskajiem paraugiem; telpas tīras zonas rezultātu atklāšanai (elektroforēze). Šīs telpas ir potenciāla piesārņojuma zona. Vēl viena izolēta teritorija ir tīra telpa testa DNS paraugu ievadīšanai mēģenēs ar reakcijas maisījumu PCR. Visbeidzot, tiek pieņemts, ka galvenais instruments - DNS pastiprinātājs - jāpārvieto uz atsevišķu, iespējams, biroja telpu.
Lai novērstu piesārņojumu ar iepriekšējo reakciju produktiem - ar ampiconiem, dažas PCR pārbaudes sistēmas deoksinukleozīdu timidīna vietā satur deoksinukleozidurīdu, kas, in vitro sintezējot, tiek ievietots tā vietā atbilstošā vietā, t.i. slāpekļa bāze timīns, kas atrodas dabiskajā DNS, tiek aizstāts ar uracilu. Uracila-DNS glikozilāze, kas pievienota reakcijas maisījumam analizējamajam materiālam, iznīcina tikai piesārņojošos fragmentus ar deoksuridīnu, bet ne dabisko analizēto DNS. satur deoksitimidīnu. Turpmākā karsēšana 94 ° C temperatūrā inaktivē šo fermentu un neietekmē PCR amplifikāciju.
Ir testēšanas sistēma, kuras pamatā ir rRNS izotermiska pastiprināšana, kurai vispirms tiek veikta DNS molekulu reversā transkripcija un sintēze. kas savukārt ir matrica turpmākai RNS molekulu sintēzei. RNS amplikoni tiek konstatēti, izmantojot hibridizācijas laikā reakcijas mēģenē, izmantojot akridīna krāsotu DNS zondi. Šī metode papildus augstai jutībai ir tā, ka tā veic analīzi vienā mēģenē, kas novērš piesārņojumu. Autori uzskata, ka šīs metodes jutīgums elpceļu paraugos sasniedz 90% ar specifiskumu 99-100%.
Jaunas noteikšanas metodes tiek īstenotas reālā laika PCR. Šīs metodes galvenokārt atšķiras ar to, ka PCR un tā rezultātu noteikšana tiek veikta vienlaicīgi vienā slēgtā caurulē. Tas ne tikai tehnoloģiski vienkāršo analīzes metodi, bet arī novērš laboratorijas telpu un testa paraugu piesārņošanu ar produktiem, kas ir pirms PCR.
Reālā laika PCR laikā rezultāti tiek atklāti fluorescences rezultātā, kas rodas, fluorinētai DNS zondei hibridizējoties ar specifisku DNS fragmentu, kas pastiprināts PCR laikā. Fluorogēno DNS zondu struktūra ir konstruēta tā, ka fluorescējošais marķieris tiek atbrīvots fermentu reakcijas rezultātā vai distancēts no fluorescences atdzesēšanas molekulas tikai specifiskās hibridizācijas laikā ar vēlamo DNS molekulu, kas pastiprināta PCR laikā. Palielinoties molekulām, kas hibridizējas ar zondi, fluorescences palielināšanās līdz nosakāmam līmenim ir proporcionāla pastiprinātā produkta molekulu skaitam. Tā kā katras PCR cikla laikā DNS fragmentu molekulu skaits ir dubultojies, cikla numurs, no kura nosaka un palielina fluorescenci, ir apgriezti proporcionāls DNS molekulu skaitam sākotnējā paraugā. Ja reakcijā kā kalibrators tiek ievadītas vairākas Mycobacterium tuberculosis attiecīgās DNS fragmenta molekulu dažādas koncentrācijas, tad DNS genomu skaitu pētāmā materiālā var aprēķināt, izmantojot datorprogrammu.
Katrs standarta paraugs tiek dublēts. Kvantitatīvs kritērijs ir minimālais PCR ciklu skaits, kas nepieciešami konstatētās fluorescences sākumam un pieaugumam. Absisss ir ciklu skaits; ordinātu ass ir fluorescences vērtība. DNS koncentrācija ir apgriezti proporcionāla ciklu skaitam, kas nepieciešams, lai parādītu fluorescenci. Labās kolonnas (21-32) logos attiecīgie koncentrācijas cikli tiek apzīmēti. Atšķirības starp 10-kārtīgām DNS fragmentu koncentrācijām 10 2 - 10 6 ml - 3,2-3,4 cikli. Diviem pacientiem IS6110 fragmentu koncentrācija bija aptuveni 10 3 / ml un 10 4 / ml. Ņemot vērā Mycobacterium tuberculosis genomā analizēto fragmentu atkārtojumu skaitu (6-20), mikobaktēriju skaits klīniskajos paraugos ir attiecīgi aptuveni 100 un 1000 šūnas.
PCR izmantošana tuberkulozes diagnostikā
PCR metode visbiežāk tiek izmantota tuberkulozes paātrinātai diagnostikai - mikobaktēriju tuberkulozes noteikšanai klīniskajos paraugos: krēpās. bronhu mazgāšana, pleiras eksudāts, urīns, cerebrospinālais šķidrums, osteolīzes punkcijas, sieviešu dzimumorgānu aspirāti un dažādi biopsijas paraugi. Pētījumā Holandē tika pētīti aptuveni 500 krēpu un bronhu tamponu paraugi no 340 pacientiem ar apstiprinātu plaušu tuberkulozes diagnozi, salīdzinošo PCR jutību, kultūru un uztriepes mikroskopiju. Analīzes jutīgums bija attiecīgi 92,6,88,9 un 52,4%. Šajā gadījumā visu metožu specifika bija aptuveni 99%.
Tika salīdzināta mikobaktēriju tuberkulozes noteikšanas efektivitāte ar uztriepes mikroskopijas metodēm, sēklas uz Lowenstein-Jensen barotni, WASTES testēšanas sistēmu un PCR analīzi. PCR jutība bija 74,4%, mikroskopija - 33,8%, sēšana vidējā blīvumā - 48,9% un ATKRITUMI - 55,8%. Vidējais atklāšanas laiks sēklām Levenshtein-Jensen vidē ir 24 dienas. ATKRITUMI - 13 dienas, PCR - 1 diena.
Tiek apspriestas arī iespējas izmantot PCR kā jutīgu un ātru metodi tuberkulozes ārstēšanas efektivitātes uzraudzībai.
Mycobacterium tuberculosis DNS noteikšana ar PCR ar efektīvu ķīmijterapiju tiek noteikta ilgāk - vidēji 1,7 mēnešus, salīdzinot ar baktēriju sekrēciju, kas konstatēta fluorescējošā mikroskopijā, un 2,5 mēnešus, salīdzinot ar bakterioloģisko izmeklēšanu.
Ekstrapulmonālās tuberkulozes diagnostika
PCR kā jutīgas metodes vērtība ir īpaši liela ekstrapulmonālajām formām, jo klīniskās rentgena metodes un tradicionālās bakterioloģiskās metodes mikobaktēriju tuberkulozes noteikšanai diagnostiskajos materiālos ir neefektīvas.
Pārbaudot urīna paraugus, PCR analīzes rezultāti bija pozitīvi 16 no 17 pacientiem ar urīnceļu aktīvo tuberkulozi un 4 pacientiem ar nieru neaktīvo tuberkulozi un 39 pacientiem ar urīnceļu sistēmas slimībām.
PCR analīzes efektivitāte tika pierādīta, pētot kaulu smadzeņu aspirātus pacientiem ar neskaidras ģenēzes drudzi, kas aizdomas par slimības tuberkulozo raksturu. Tuberkulozes limfadenīta diagnosticēšanai bērniem tika pētīti 102 punkcijas aspirāti un 67 bērnu ar biopsiju limfadenītu biopsijas paraugi. Tika iegūti pozitīvi rezultāti: reālā laika PCR - 71,6%. fluorescences mikroskopija - 46,3%. kultūras studijas - 41,8%. Pētījumā ar 50 limfmezglu biopsijām pacientiem ar kaķu skrāpējumiem, visi rezultāti bija negatīvi. Tādējādi tika pierādīta PCR analīzes 100% specifika. Tajā pašā darbā limfmezglu punkcijas biopsija parādīja iespēju atklāt M. avium.
Kā zināms, sieviešu dzimumorgānu tuberkulozes diagnosticēšana ar neauglību ir viena no grūtākajām diagnozes problēmām. Pētījumā, kurā tika izmantota endometrija biopsiju, endometrija aspirātu un Douglas telpas šķidruma paraugu PCR, 14 (56%) no 25 pacientiem, kuri tika pārbaudīti laparoskopiski ar aizdomām par tuberkulozi, bija pozitīvi rezultāti. Izmantojot uztriepes mikroskopijas un kultūras pētījumus, ieguva attiecīgi 1 un 2 pozitīvus rezultātus. Šie gadījumi bija arī pozitīvi PCR. Lielākā daļa PCR pozitīvo rezultātu bija saistīti ar gadījumiem ar raksturīgām tuberkulozes pazīmēm saskaņā ar histoloģisko izmeklēšanu; mazāk, ja ir aizdomas, ka laparoskopijā ir tuberkuloze. Tikai viens pozitīvs PCR analīzes rezultāts tika iegūts bez laparoskopiskiem datiem par tuberkulozi.
Diagnosticējot tuberkulozes ekstrapulmonālās formas, ārstiem bieži ir jautājums par patogēna noteikšanu asins paraugu PCR pētījumā. Literatūras dati liecina, ka Mycobacterium tuberculosis DNS noteikšana no asins paraugiem ir iespējama ar progresējošu HIV infekcijas formu palīdzību. Mycobacterium tuberculosis DNS tika konstatēta tikai dažu orgānu vispārinātas tuberkulozes gadījumā pacientiem ar transplantētu nieru un imūndepresiju.
Mikobaktēriju identifikācija
PCR metode var būt diezgan efektīva, lai ātri identificētu mikobaktēriju tuberkulozes kompleksu un dažus ne-tuberkulozes mikobaktēriju veidus pēc to sākotnējās augšanas. Šajā gadījumā PCR izmantošana var ietaupīt 7-10 dienas, kas nepieciešamas turpmākajai kultūras identifikācijai. pozitīvs rezultāts. Pētījumi ar PCR ir tehniski ļoti vienkārši, jo nav nepieciešama sarežģīta paraugu sagatavošana klīniskajam materiālam, lai panāktu augstu jutību. Pētījumā par 80 pozitīvām kultūrām šādā testa sistēmā (MB VasT. No Organon kompānijas) visi pozitīvie PCR analīzes rezultāti bija stingri specifiski un tika veikti 1 dienu. Lai identificētu citus mikobaktēriju veidus, kad tie iegūti kultūrā, patogēnu DNS hibridizējas ar specifiskiem DNS zondēm, kas marķētas ar akridīnu, un celmus atklāj ar ķīmiluminiscences izpausmi, izmantojot ķīmiluminometru vai nitrocelulozes sloksnes ar vizuālu novērtējumu pēc hibridizācijas. Ar šo komplektu tiek identificēts ierobežots sugu skaits: Mycobacterium tuberculosis komplekss. M. avium, M. avium komplekss, M. kansasii un M. gordonae.
A.Telenti et al. Viņi arī izstrādāja salīdzinoši vienkāršu un lētu klīniski nozīmīgu mikobaktēriju sugu identifikācijas metodi, pamatojoties uz PCR un turpmāku apstrādi ar diviem restrikcijas enzīmiem (fermentiem, kam piemīt īpašības, kas ļauj samazināt DNS molekulu noteiktās vietās). Kad tas tiek pastiprināts, DNS fragments. kodē siltuma šoka proteīnu (65 kDa), pēc tam 439 nukleotīdu pāru DNS fragmentu, kas iegūts ar PCR, apstrādā atsevišķi ar diviem fermentiem - Bste II un Hae III. Pēc tam, izmantojot agarozes gēla elektroforēzi, tiek iegūti divi iegūtie produkti, nosakot to izmērus (nukleotīdu pāru skaitu), izmantojot standarta DNS fragmentu kopumu (molekulārās DNS marķierus), kuru garums ir no 100 līdz 1000 nukleotīdu pāriem. Katrā noteiktā sugā (M. tuberculosis, M. avium, M. intracellulare, M. kansasii, M. fortuitum) katram restrikcijas enzīmam ir atrodami 2 vai 3 dažāda lieluma DNS fragmenti. Dažādu iegūto DNS fragmentu kombinācija ļauj šīm sugām atšķirt sevi.
Tiek izstrādāta bioloģisko DNS mikroshēmu tehnoloģija. kas palīdzēs noteikt vairāk nekā 100 mikobaktēriju veidus vienā pētījumā.
Sugu identifikāciju var veikt arī ar 16S rRNS mainīgā reģiona PCR amplifikāciju, kam seko amplikonu secība, salīdzinot ar attiecīgo primāro struktūru, kas ļauj identificēt vairāk nekā 40 mikobaktēriju sugas.
Izmantojot PCR, var veikt arī sugu identifikāciju Mycobacterium tuberculosis kompleksā, ieskaitot M. bovis un M. bovis BCG diferenciāciju. Šim nolūkam tiek analizēta noteiktu gēnu klātbūtne vai neesamība RD1 genomajos reģionos. RD9 un RD10. M. bovis BCG nav RD1, bet tā ir virulentās sugās, ieskaitot M. bovis.
Mycobacterium tuberculosis zāļu jutības noteikšana, izmantojot PCR
Molekulāro ģenētisko metožu uzdevumi, lai noteiktu Mycobacterium tuberculosis medikamenta jutību vai rezistenci, ir samazināti, lai noteiktu mutācijas noteiktās zināmo gēnu nukleotīdu sekvencēs. Galvenās metodes balstās vai nu uz šo secību tiešu nolasīšanu (sekvencēšanu) pēc amplifikācijas, vai uz biotīnu iezīmētu DNS fragmentu hibridizāciju, kas pastiprināti PCR laikā ar DNS zondēm. Abi varianti liecina par to, ka ir jāidentificē nukleotīdu sekvences, kas, lietojot DNS zondes, noved pie nitrocelulozes membrānas hibridizācijas vai defektēšanas, izmantojot fermentu konjugātu (streptavidīna-sārmainā fosfatāze) - LIPA-Rif-TB metodi.
Fluorescences mērīšanas metodi DNS mikroshēmās, kas lokāli piestiprinātas pie mikrosītiem, kas papildina zināmās mutācijas PCR pastiprinātos gēnu reģionos, kuri ir atbildīgi par zāļu jutību vai rezistenci, sauc par mikrobiochip metodi. Pamata algoritms šī pētījuma veikšanai ir šāds. Pēc DNS izolācijas no mikobaktēriju klīniskā parauga vai kultūras ir nepieciešams veikt PCR, lai pastiprinātu atbilstošos groV gēna fragmentus, kas ir atbildīgi par zāļu jutību pret rifampicīnu, vai katG un inhA gēnus, kas kodē mikobaktēriju proteīnus, kas ir atbildīgi par izoniazīda jutību. PCR rezultātus novērtē, izmantojot agarozes gēla elektroforēzi, kas apstiprina atbilstošo vēlamo DNS fragmentu sagatavošanu. Tam seko 2. kārta PCR, lai ievadītu fluorescējošo marķējumu DNS. PCR rezultātus atkal apstiprina ar gēla elektroforēzi. Pēc tam tiek veikta hibridizācija (inkubācija pa nakti), kam seko iegūto materiālu mazgāšana biocipā, kas ir liels īsu DNS ķēžu skaits (zondes), kas piestiprinātas pie nelielas stikla plāksnes, kas papildina mikobaktēriju jutīgās tuberkulozes nukleotīdu sekvences iespējamo mutāciju punktos. kā arī mutantu sekvences, kas ir atbildīgas par zāļu rezistenci. DNS zondes izvietojums uz plāksnes ir stingri noteikts, un tiek noteikts novērotā fluorescences līmenis hibridizācijas laikā, lai noteiktu rezultātu, izmantojot īpašu lasītāju. Šajā sakarā analīzes rezultātus nosaka, izmantojot īpašu datorprogrammu.
Pēdējos gados ir izstrādātas arī alternatīvas metodes Mycobacterium tuberculosis narkotiku jutības noteikšanai, pamatojoties uz reāllaika PCR tehnoloģiju, ļaujot šos pētījumus veikt slēgtā caurules režīmā.
Att. 13-13 atspoguļo Mycobacterium tuberculosis klīnisko kultūru analīzes rezultātus, nosakot zāļu rezistenci pret rifampicīnu, izmantojot reālā laika PCR: 218 - kontrolparaugu (jutīgs pret rifampicīnu); 93 - pozitīva Ser-Trp TCG-TGG mutācijas kontrole; 4482 - pozitīva kontrole Ser-Leu TCG-TTG mutācijai; 162-322 - eksperimentālie paraugi. Kinetisko pastiprināšanas līkņu aprēķins 4 kanāliem: kanāls 1: 393 - pozitīva kontrole Ser-Trp TCG-TGG mutācijai; kanāls 2: 4482 - pozitīva kontrole Ser-Leu TCG-TTG mutācijai; 162, 163, 172, 295 - eksperimentālie paraugi; 4. kanāls: visu eksperimentā iesaistīto paraugu kinētiskās pastiprināšanas līknes. Pozitīva kontroles pastiprināšanas reakcija. Secinājumi: analīzes rezultāti atklāja šādas mutācijas, kas nosaka rezistenci pret rifampicīnu: paraugos 162,163,172,295 - Ser-Leu TCG-TTG. To pašu principu izmanto, lai noteiktu pretestību pret izoniazīdu katG un inhA gēniem, kas nosaka visbiežākās mutācijas.
Muskobaktēriju tuberkulozes celmu identifikācija
Vispētītākā Mycobacterium tuberculosis identifikācijas metode ir tehnoloģija, ko sauc par restrikcijas fragmenta garuma polimorfismu (RFLP vai RFLP angļu valodā) un kas balstās uz Mycobacterium tuberculosis DNS fragmentēšanu (ierobežošanu) ar Pvu II enzīmu un pēc tam iegūto fragmentu hibridizāciju ar noteiktām specifiskām DNS sekvencēm. tā atkārtotais elements ir IS6110. Intraspecific variabilitāte tiek realizēta, pateicoties atšķirīgajam IS6110 atkārtojumu skaitam un to atrašanās vietai DNS. kā arī attālumu atšķirība starp noteiktiem uzbrukuma punktiem fermentu ierobežojumiem (restrikcijas vietām) un elementam IS6110. Šī tehnoloģija ir ļoti sarežģīta un laikietilpīga. Pēc DNS, kas izolēta no Mycobacterium tuberculosis kultūras, ar restrikcijas enzīmu, apstrāde tiek veikta ar gēla elektroforēzi, tad dažāda garuma DNS fragmenti tiek pārnesti uz nitrocelulozes membrānu, hibridizēti ar IS6110 fragmentiem un rezultāti tiek konstatēti, izmantojot enzīmu reakciju. Iegūtais joslu raksturojums raksturo specifiskas Mycobacterium tuberculosis celms DNS. Izmantojot datora analīzi, atklājās celmu identitāte vai afinitāte. Lai gan RFLP metode ir visdiskriminējošākā, t.i. atklāj lielāko atšķirību skaitu analizētajos celmos, tas ir neefektīvs ar nelielu skaitu (mazāk nekā 5) IS6110 atkārtojumu, kas novēroti dažos celmos. Att. 13-14 attēlo celmu RFLP rakstīšanas rezultātus.
Alternatīva var būt spoligotipu noteikšanas metode (spoligotipizēšana) - DNS starpliku secību polimorfisma analīze - starp starp tiešo DR reģiona atkārtošanos. Veicot celmu spoligotipizēšanu, PCR tiek veikta ar primeriem, kas ierobežo DR reģionu, pēc tam veidojas dažāda garuma fragmenti, kas hibridizējas ar DNS mainīgajiem starpreģioniem. Ir parādīta DR reģiona distancējošo secību analīze. Pēc pētnieku domām, tas ir vienkāršāks, produktīvāks un piemērots primārajai celmu pārbaudei un provizoriska epidemioloģiska analīze, kā arī tieši klīniska materiāla izpēte.
Acīmredzot efektīvāka un tehnoloģiski pieejamāka metode ir VNTR (angļu valodas vārdu saīsinājums) vai metode Mycobacterium tuberculosis DNS specifisko tandēmu atkārtojumu mainīgā skaita noteikšanai. Šī metode ir balstīta tikai uz PCR izmantošanu un neprasa papildu manipulācijas. Tā kā tandēma atkārtojumu skaits dažādos celmos un dažādos lokos ir atšķirīgs, dažāda lieluma fragmenti tiek noteikti un analizēti, iegūstot PCR produktu elektroforegramu. Pēc pētnieku domām, izmantojot VNTR, tika panākta lielāka celmu diskriminācijas pakāpe nekā izmantojot RFLP metodi.
Pēdējos gados liela uzmanība ir pievērsta Mycobacterium tuberculosis W-Beijing ģimenes celmu izplatībai (dažreiz tos sauc par Pekinas celmu), kas lielā mērā ir rezistenti pret narkotikām.
Pamatprasības molekulārās bioloģiskās izpētes kvalitātei
PCR pamatdokumenti
Krievijas Veselības ministrijas rīkojumi: Nr. 45, 2000. gada 7. februāris. Nr. 109, 2003. gada 21. marts. Nr. 64, 2000. gada 21. februāris. Metodiskās vadlīnijas: 1.3.1888-04 “Darba organizēšana PCR pētījumos ar patogēno bioloģisko inficēto materiālu III-IV patogenitātes grupu aģenti "; 1.3.1794-03 "Darba organizēšana PCR pētījumos ar I-II patogenitātes grupu mikroorganismiem inficētiem materiāliem". 2003; 3.5.5.1034-01 "I-IV patogenitātes grupu baktērijām inficētā materiāla dezinfekcija, izmantojot PCR metodi", 2001. Pielikums 11. instrukcijai par vienotu mikrobioloģisko pētījumu metodēm tuberkulozes atklāšanai, diagnosticēšanai un ārstēšanai.
Personāls
Molekulāros bioloģiskos pētījumus var veikt klīniskās laboratorijas diagnostikas ārsti, bakteriologi, virologi, klīniskās diagnostikas laboratorijas biologi, kā arī speciālisti ar vidējo medicīnisko izglītību, kuri ir specializējušies un apmācīti iepriekš.
Ierīces telpu laboratorija
Ir nepieciešamas šādas laboratorijas iekārtas:
- Paraugu apstrādes apgabals ir laboratorija, kas pielāgota darbībai ar patogēnuma III-IV grupas infekcijas līdzekļiem saskaņā ar metodoloģiskajām vadlīnijām 13.1888-04.
- Reakcijas maisījumu sagatavošanas zona PCR - laboratorijas telpa, kas nodrošina aizsardzību pret iekšējo laboratorijas piesārņojumu - "tīro" zonu.
- Ja PCR produktu analīzei izmanto elektroforēzes metodi vai hibridizāciju. laboratorijas telpai, kurā pavairotie DNS fragmenti tiek izvadīti no amplifikācijas caurules un tādējādi var tikt izlaisti vidē saskaņā ar PCR laboratoriju prasībām (Vadlīnijas 1.3.1794-03, pamatnostādnes 1.3.1888-04), jābūt pilnīgi izolēti no iepriekšējos punktos norādītajām telpām. Jāizslēdz kustība no elektroforēzes zonas uz paraugu apstrādes zonu un jebkura personāla, aprīkojuma, materiālu un priekšmetu „tīro” zonu, kā arī gaisa pārnesi caur ventilācijas sistēmu vai caurvēja rezultātā. Šī zona nav nepieciešama PCR produktu fluorimetriskai noteikšanai.
- Dokumentācijas un rezultātu apstrādes telpa ir aprīkota ar datoriem un nepieciešamo biroja aprīkojumu. Šajā telpā var atrast iekārtas, lai atklātu PCR produktus, neatverot cauruli. - fluorescējoši PCR detektori un termocikeri reāllaika PCR.
Sanitārās un epidemioloģiskās prasības krēpu primārajai ārstēšanai ir līdzīgas standarta mikrobioloģiskajām prasībām strādāt ar tuberkulozes mikobaktērijām.
PCR diagnostikas laboratorijas aprīkojuma komplekts
Laboratorijas paketē ietilpst iekārtas šādām telpām.
- paraugu sagatavošanas telpā ir šādas iekārtas: II lamināra aizsardzības klase "SP-1.2": cietvielu termostats ar apsildāmu vāku Eppendorf tipa caurulēm; mikrocentrifūga pie 13 000 apgr./min; centrifūga ("Vortex"); ledusskapis ar temperatūras diapazonu no -20 ° C līdz +10 ° C; mainīgās tilpuma pipetes no Proline sērijas; sūknis ar OM-1 kolbas slazdu; pipetes statīvs; statīvs darbavietā 200x0,5 ml; statīvs darbavietā 50x1,5 ml; plaukti uzglabāšanas caurulēm 80x1,5 ml;
- telpa reakcijas maisījuma pagatavošanai: aizsargkameras PCR kaste (“Laminar-110 cm”); Vortex centrifūga; mainīgās tilpuma pipetes no progresīvās līnijas; pipetes statīvs; trijkāja darbavieta 200x0,2 ml; plaukti uzglabāšanas caurulēm 80x1,5 ml; ledusskapis ar temperatūras diapazonu no -20 o C līdz + 10 o C;
- elektroforēzes telpa: kamera horizontālai elektroforēzei; barošanas avots; transilluminators;
- DNS pastiprinātājs vai nukleīnskābes analizators (reālā laika PCR) ar datoru un programmatūru; var ievietot jebkurā brīvajā telpā. Ja izmantojat PCR tehnoloģiju reālā laikā. nav nepieciešama elektroforēzes telpa.
Ārējā kvalitātes kontrole
Lai iegūtu pārliecību par objektīvi ticamu rezultātu iegūšanu, laboratorijām jāpiedalās laboratorijas pētījumu ārējās kvalitātes novērtēšanas sistēmā.
Kvalitātes kontroles sistēmas dalībnieki saņem; 12 ampulas ar liofilizētām baktēriju šūnu suspensijām, no kurām divas satur E. coli E. coli, 3 ampulas ar mikobaktēriju tuberkulozi (avirulents celms) pie koncentrācijas 10 2 / ml; 3 ampulas ar līdzīga celma šūnām ar koncentrāciju 10 4 / ml; 2 ampulas ar ne-tuberkulozu mikobaktēriju M. avium-intracellulare un M. kansasii koncentrācijā 10,5 / ml.
Sadalītie ārējās kvalitātes novērtēšanas testi ir iepriekš pārbaudīti divās neatkarīgās laboratorijās ar plašu pieredzi šajā jomā.
Metode ļāva identificēt daudzus slimus cilvēkus, samazināt saslimstības, mirstības statistiku.
Mikobaktēriju un krēpu mikroskopijas sēšana saskaņā ar Zil-Nelson ļauj droši diagnosticēt infekciju. Problēma izraisa precīzu krēpu ņemšanu tieši no skartā bronhu. Uz tuberkulozes procesa fona tiek ietekmēta nozīmīga bronhu koka daļa. Pēc baktēriju inokulācijas ir iespējams pārbaudīt patogēna jutību pret antibiotiku.
Pēc diagnostikas rezultātu analīzes, ko veica ftisiatrologi, kļuva skaidrs, ka Koch stieņa neesamība nav izdalīta, tas nenozīmē organisma infekcijas neesamību. Cēlonis var tikt noteikts pēc otrā, trešā, ceturtā materiāla.
Moderns diagnostikas metodes (dst, Quantiferon tests) identificēt mikobaktērijas ar aktīvo slimības gaitu. Mikobaktēriju klātbūtnē limfmezglu iekšienē ar slimības ekstrapulmonālām formām, testi visbiežāk ir negatīvi.
Savlaicīga diagnoze ir pamats nopietnu komplikāciju un slimības bīstamu seku novēršanai.
Mūsdienu metodes
Klasiskās tuberkulīna diagnozes aizstāšana ir diaskintests (dst). Saskaņā ar jaunākajiem noteikumiem pētījumā jāaizstāj standarts Mantoux tests, kas ļāva noteikt daudzus saslimstības un infekcijas gadījumus iedzīvotāju vidū.
Diaskintesta būtība, kā arī tuberkulīna diagnoze ir saistīta ar tuberkulozes patogēnu proteīnu subkutānu ievadīšanu. Atbildot uz injekciju, rodas paaugstinātas jutības reakcija ar specifiskām ādas izmaiņām: apsārtums, indurācija, čūlas.
Pozitīvs Diaskintest rezultāts ir raksturīgs pacientiem ar aktīvu slimības gaitu. Ja inficēts vai paaugstināts alerģiju pētījums būs negatīvs. Dst negatīvā ietekme var būt spēcīgas imunitātes rezultāts, bet, ja persona ir inficēta.
Salīdzinot ar Mantus, Diaskintest ir daudzpusīgāks un jutīgāks veids, kā diagnosticēt tuberkulozi. Infekcijas atklāšanas trūkums prasa to lietot vienlaikus ar tuberkulīna diagnozi.
Neskatoties uz klīnisko pētījumu rezultātiem, zinātnieki apgalvo, ka šī metode ir vispārēja daudzveidība un jutīgums, pētījumu nevar uzskatīt par universālu diagnostikas risinājumu.
Testu ir izstrādājuši Sechenov Research Institute akadēmiķi Alerģiju trūkums, lietojot diaskintestu, ir saistīts ar sugai specifisku tuberkulozes proteīnu subkutānu ievadīšanu. Pēc to ieviešanas nosaka ādas reakcija apsārtuma, plombu veidā.
Kas ir kvantferona tests
Kvantferona testu novērtē pēc pacienta asinīs uzņemšanas. Procedūras mehānisms ir noteikt gamma-interferonu, ko atbrīvo T-limfocīti pēc tikšanās ar mycobacterium tuberculosis. Testi nosaka tuberkulozes olbaltumvielas, kas satur ne tikai cilvēku un liellopu baktērijas. Kvantferona testu var izmantot arī citu mikobaktēriju izraisītu mikobaktēriju diagnosticēšanai, kas veido specifiskas izmaiņas roentgenogrammā. Testa rezultātu nosaka vairākās caurulēs, kas palielina metodes diagnostisko jutību.
PCR bērnu tuberkulozes diagnosticēšanai
Polimerāzes ķēdes reakcija ir precīza, bet dārga metode tuberkulozes diagnosticēšanai. PCR tiek veikta pēc bronhoskopijas.
Pēc negatīvu rezultātu saņemšanas ir racionāli veikt polimerāzes ķēdes reakciju. Rezultātus novērtē pēc Mycobacterium tuberculosis trīs reizes ilgas krēpu audzēšanas. Visvairāk labvēlīgos apstākļos patogēna identifikācija norāda uz infekciju. Ķimoprofilakses mērķis ļauj izvairīties no aktīva tuberkulozes procesa Koch sticks klātbūtnē.
Saņemot mikroorganisma celmu, ir iespējams sēt antibiotiku jutību. Antibiotiku noteikšana, kas var nogalināt mikroorganismus, ļauj novērtēt, kuras zāles infekcijas ārstēšanai.
PCR bērniem tiek veikta ar negatīvu sēšanas rezultātu, bet, ja ir saliekt tuberkulīna testsinficēšanās radioloģisko pazīmju vizualizācija, pašreizējās infekcijas klīnisko simptomu identificēšana.
Polimerāzes ķēdes reakcija nodrošina augstu precizitāti (apmēram 99%). Metode balstās uz nukleīnskābes pastiprināšanu. Mikobaktērijām, vīrusiem un citiem mikroorganismiem ir unikālas nukleotīdu sekvences. Viņu diagnoze ļauj noteikt slimības izraisītāju.
PCR jutīgums bērniem ir mazāks nekā pieaugušajiem. Praksē atklājās šādas polimerāzes ķēdes reakcijas pazīmes bērnam:
- Specifiskums - 80-100%;
- Jutīgums - 25-80%.
Neskatoties uz metodes augsto precizitāti, negatīva rezultāta iegūšana nenozīmē, ka bērniem nav tuberkulozes. Racionālāka metodes izmantošana pacientiem ar imūndeficītu. Diagnozējot ekstrapulmonālo tuberkulozes infekciju.
Mutiskās tulkošanas kļūdas nosaka pētījuma materiālu savākšanas un sagatavošanas pārkāpumi.
PCR negatīvā rezultāta iemesli tuberkulozes diagnostikā
Mikobaktēriju izplatīšanās organismā ar limfogēno (caur limfātiskajiem traukiem) un hematogēnu (caur asinsriti) nodrošina daudzu audu kolonizāciju, ekstrapulmonālu infekcijas fokusu parādīšanos.
Kad rentgenoloģiski nosaka plaušu iznīcināšanas (iznīcināšanas) centrus, nav nepieciešams PCR. Pieaugušajiem, izmantojot rentgenogrāfiju, ir iespējams identificēt tekošās formas ar augstu uzticības pakāpi.
Bērniem PCR pētījums biežāk tiek izmantots sakarā ar mikobaktēriju slēpto lokalizāciju limfmezglos, kas rada negatīvus rezultātus, lietojot citas diagnostikas metodes. Ar baktēriju kultūru pietiek ar aptuveni 10 mikroorganismu noteikšanu. Jāatceras, ka ne visi ir atbildīgi par aktīvo plaušu tuberkulozi.
Pareizai PCR diagnozei, baktēriju sēšanai, DST jāievēro prasības:
- Glabāt materiālu sterilās caurulēs;
- Novērst citu baktēriju iekļūšanu;
- Veicot transportēšanu, ievērojiet personīgo higiēnu, lai nepieļautu biomateriāla nokrišanu uz ķermeņa, sejas un elpceļu.
Saglabā asinis kopā ar konservantu EDTA. Katrai laboratorijas analīzei ir unikālas materiālu sagatavošanas iezīmes, ar kurām ir zināmi eksperti.
Inovatīvas diagnostikas metodes
Infekcijas agrīna atklāšana ļauj laicīgi ķīmiski novērst smagu slimību.
Klīnikas dzēšana bērnībā, nepietiekami testa rezultāti, analfabētu analīzi par paraugu novērtēšanu neļauj savlaicīgi pārbaudīt infekciju. Lai novērstu zīdaiņu saslimstību, ir nepieciešama rūpīga rezultātu analīze un iespēja noteikt diagnozi agrīnā stadijā.
Mūsdienīga metode tuberkulozes diagnosticēšanai bērniem - TAB-TM noteikšana
Reakciju uz T-šūnu marķiera definīciju bērniem, ko sauc par “TAB-TM”, raksturo augsta jutība. Metodes būtība ir noteikt konkrētu diferenciācijas kopu (CD-27), kas lokalizēts T-limfocītu virsmā. Pēc šī faktora izolēšanas citokīni tiek krāsoti ar citometriju.
Metode ir aprakstīta literatūrā kopš 2014. gada. Novērojumu rezultāti norāda uz metodes augsto jutību. TAB-TM noteikšana ir izteikta metode tuberkulozes diagnosticēšanai ar krēpu pārbaudi.
Asins tests tuberkulozei - kas liecina
Sākotnējā stadijā tuberkulozes infekcija turpinās bez specifiskiem klīniskiem simptomiem. Laboratorijas diagnoze bērniem tas kļūst iespējams, kad Kochas zizlis pavairojas.
Kādas šūnas tiek novērtētas tuberkulozes procesa laikā laboratorijas asins analīzē:
- Sarkanās asins šūnas ir sarkanās asins šūnas, kas ir atbildīgas par skābekļa transportēšanu uz audiem. Ar vieglu plūsmu plaušu tuberkuloze no sarkano asnu patoloģisko izmaiņu sekas netiek izsekotas. Destruktīvas koncentrācijas klātbūtne veicina asiņošanu ar asins anēmiju. Stāvoklis attīstās ar zarnu trakta iekaisumu. Retikulocītu skaits patoloģijas fonā palielinās vairāk nekā par 1%;
- Leukocīti palielinās ar jebkuru infekciju. Leukocitozi papildina leukogrammas nobīde pa kreisi. Segmentēto neitrofilu skaita pieaugumu var izsekot sākumposmā. Smagā tuberkulozē ar strutainu saplūšanu, imūndeficīta stāvokļiem novēro leikopēniju (asins leikocītu skaita samazināšanās). Tajā pašā laikā palielina limfocītu saturu (vairāk nekā 20%);
- Eozinofiliju var izsekot līdz sākotnējam posmam. Stāvoklis rodas, kad tuberkulozi infiltrējas dažādos orgānos. Smaga tuberkuloze ar sabrukumu pieaugušajiem izraisa pilnīgu eozinofilu trūkumu;
- Basofila uzlabošana.
Laboratoriskās tuberkulozes pārbaudes nav specifiskas bērniem vai pieaugušajiem. Šādas izmaiņas ir raksturīgas daudzām baktēriju vai vīrusu infekcijām.
Hemogrammas indikatori dod interesi ftisiatrologiem noteikt tuberkulozes infekcijas stadiju.
Aktīvā infiltrācijā leikocitozi var izsekot, palielinoties neitrofilu skaitam. Šūnās parādās patoloģisks smiltis, kas norāda uz asins saindēšanos.
Sadalīšanās centri samazina eozinofilu, neitrofilu, jauno formu, limfocītu skaitu. Ja izplatās, notiek absolūtā monocitoze. Pret rezorbciju palielinās limfocītu un eozinofilu skaits.
Centru nostiprināšanā hemogrammai nav raksturīgas izmaiņas.
Bērnu tuberkulozes testi: tuberkulīna diagnoze
Ilgu laiku pthisiatricians iestudēja Mantoux reakciju. Šādi tuberkulozes testi ļāva atklāt ne tikai aktīvo infekciju, bet arī infekciju. Parauga būtība bija subkutāna tuberkulīna injekcija - viela, kas izraisīja organisma alerģiju. Mīklas materiāls iegūts no Micobacterium Bovis. Pēc subkutānas injekcijas tiek iegūts papule, kas atspoguļo organisma reakciju uz mikobaktēriju iekļūšanu:
- Normāla papula - izmērs no 5 līdz 16 mm;
- Ja nav reakcijas - imūnsistēmas vājināšanās, mikobaktēriju trūkums;
- Liela papule - baktēriju antigēnu klātbūtne, nonākot saskarē ar tuberkulozes nesēju.
Metode nav uzskatāma par uzticamu, jo ir daudz nepatiesu pozitīvu reakciju. Ja rodas apšaubāmi rezultāti, nepieciešams apstiprinājums PCR. Ar diaskintesta (dst) parādīšanos situācija ir mainījusies. Kombinēta metožu izmantošana ļauj iegūt ticamākus rezultātus.
Klasiska tuberkulozes "TB" diagnoze
Pthisiatricians par tuberkulozes diagnozi bērniem un pieaugušajiem izmanto šādus testus:
- Pacienta vēstures izpēte (saskare ar pacientu vai tuberkulozes bacillus nesēju). Sociālo riska faktoru identificēšana palīdz ieteikt iespējamo infekciju;
- Tuberkulīna jutības novērtējums (Mantoux tests) ar PPD tuberkulīnu 5-10 TE devā. Rezultāta novērtēšana tiek veikta 48-72 stundu laikā;
- Rentgena izmeklēšanu veic bērniem un pieaugušajiem, kuriem ir aizdomas par tuberkulozi, tuberkulīna testu līkumu;
- Bakterioloģiskā kultūra ir neapstrīdams Mycobacterium tuberculosis izraisītas infekcijas pierādījums. Pareiza krēpu savākšana, patogēna noteikšana kuņģa mazgāšanā, tuberkulozes testus var uzskatīt par pozitīviem. Kochas zizlis ir atrodams strutainos abscesos, limfmezglos, ascīta izsvīdumā, pleiras eksudātā, urīnā, cerebrospinālā šķidrumā;
- Eritrocītu sedimentācijas ātrums palielinās ar jebkuru infekciju, ieskaitot tuberkulozi;
- PCR ļauj noteikt specifisku patogēnu, bet pētījums ir dārgs;
- Diaskintest nosaka plaušu tuberkulozi, bet bieži izraisa negatīvu rezultātu infekcijas ekstrapulmonālajā lokalizācijā.
Mūsdienīga tuberkulozes diagnostika, izmantojot metožu kompleksu, ļauj noteikt mikobaktēriju organismā ar augstu ticamības pakāpi. Izmantojot esošās metodes, tiek atklāts aktīvs process vai infekcija. Mums ir nepieciešams laiks, lai sazinātos ar ekspertiem!
V.Yu. Mishin
Pacientu identifikācija - daļa cīņas pret tuberkulozemērķis ir noteikt šīs slimības gadījumus sabiedrībā.
Pacientu, kas pieteikušies uz vispārējo medicīnisko tīklu (LU OMS), medicīniskā personāla medicīniskā personāla pārbaudi pacientu ar tuberkulozi atklāšanā veic pacienti, kas pieprasīja medicīniskā aprūpe, kā arī parastās profilakses pārbaudēs dažām iedzīvotāju grupām.
Tuberkulozes pacientu noteikšanai jābūt agrīnai vai vismaz laikus. Pacientu identificēšana ar progresīvām tuberkulozes procesa formām rada lielas grūtības ārstēšanā, jo ir grūti dziedēt tuberkulozes fokusu pat ar modernām ārstēšanas metodēm.
Ilgstošs tuberkulozes kurss pacientiem, kas nav iekļauti tuberkulozes slimnīcā, rada lielu epidemioloģisku risku apkārtējiem iedzīvotājiem, īpaši ar masveida un bagātīgu biroja sekrēciju.
Galvenās metodes tuberkulozes noteikšanai paliek:
- radiācijas diagnostika;
- bakterioloģiskā diagnoze;
- tuberkulīna diagnoze.
Visas šīs metodes tiek izmantotas indivīdiem ar paaugstinātu tuberkulozes risku, kas atrodas OMS direktorātā, kuri dodas uz klīnikām un dodas uz slimnīcu, lai ārstētu slimības simptomus, par kuriem ir aizdomas par tuberkulozi. Tuberkuloze skar dažādus orgānus un sistēmas, tāpēc, lai noteiktu ekstrapulmonālo tuberkulozi, atkarībā no slimības atrašanās vietas tiek izmantotas īpašas pārbaudes metodes.
Daudzus gadus ir bijis pamats pieaugušo elpošanas tuberkulozes atklāšanai rentgena metode. Tuberkulozes agrīna atklāšana tika veikta, izmantojot fluorogrāfiju, kas katru gadu tika veikta visiem pieaugušajiem, biežāk kā reizi 1-2 gados.
Masveida rentgena izmeklējumi aptvēra lielāko daļu iedzīvotāju un ļāva identificēt pacientus ar elpošanas ceļu tuberkulozi salīdzinoši agrīnā attīstības posmā. Izmantojot fluorogrāfisko metodi, pacienti tika identificēti un atlasīti galvenokārt ar ierobežotiem lokāliem procesiem fokusa tuberkulozes, ierobežotu infiltrātu, izplatīšanās un tuberkulozes veidā. Slimības klīniskās izpausmes šiem pacientiem bija vieglas vai nav.
Masu fluorogrāfija kā metode tuberkulozes noteikšanai tika izstrādāta pirmsbakteriālā periodā, kad, neraugoties uz visiem mēģinājumiem ārstēt, kopīgo destruktīvo procesu prognozēšana ar baktēriju sekrēciju joprojām bija ļoti apšaubāma. Tajā laikā vairāk nekā 50% šo pacientu nomira piecu gadu laikā pēc diagnozes.
Bija steidzami nepieciešama metode slimības atklāšanai agrīnā stadijā, kad process plaušās tika ierobežots bez dobumiem un baktērijām, ko varēja konstatēt tikai radiogrāfiski.
Ķīmijterapijas attīstība ir tikai apstiprinājusi nepieciešamību agrīnā un savlaicīgā elpošanas orgānu tuberkulozes atklāšanā, jo ir daudz vieglāk panākt pilnīgu klīnisko izārstēšanu nelielām slimības formām nekā ārstēt parastos dobuma procesus.
Mūsdienu apstākļos ar in narkotiku pretestība MW pieaugumu un ir ierobežots skaits galvenokārt ir ļoti vecas, anti-TB zāļu, Fluoroskopijā nozīme kā metode agrīnas un savlaicīgā atklāšanā plaušu tuberkulozes palielinās ievērojami, kā ārstējot uzlabotas formas zālēm rezistentas plaušu tuberkuloze ir dārga, ko izraisa ne tikai kombinēta ķīmijterapija ar dārgām rezervju zālēm, bet arī dārgas ķirurģijas izmantošana intervences.
Pacienti ar šādām slimības formām bieži nejūtas slikti, saglabāja savu spēju strādāt. Pārbaudes gaitā vispirms tika veikti elpošanas sistēmas rentgenstari, lai noskaidrotu ar fluorogrāfiju saistītās izmaiņas. Šīs kategorijas pacientu ārstēšanas efektivitāte bija ļoti augsta.
Iedzīvotāju masveida fluorogrāfiskā skrīnings ir visefektīvākā kontroles metode, jo savlaicīga un savlaicīga ierobežotu respiratorās tuberkulozes formu atklāšana un to efektīva ārstēšana ir galvenie faktori, kas samazina infekcijas rezervi iedzīvotāju vidū.
Turklāt regulāri fluorogrāfija seansi, lai atklātu šādus elpošanas orgānu slimības, piemēram, plaušu vēzis, sarkoidoze, limfomas un citu limfoproliferatīvo slimībām, kas sākotnējā stadijā ir asimptomātiski un labi reaģēt uz ārstēšanu. Optimāli ir veselas populācijas ikgadējie fluorogrāfiskie izmeklējumi.
Fluoroskopijas gadā obligāti jāveic "obligātu kontingents", lai skrīningu tuberkulozes (veselības aprūpes darbinieki, bērnu darbinieku un valsts iestādēm, ēdināšana, pārtikas veikali, sabiedriskais transports, uc).
Pēdējos gados ir ievērojami samazinājušies populācijas profilaktiskie fluorogrāfiskie pētījumi, kas ir izraisījis ļoti ievērojamu tuberkulozes slimnieku skaita samazināšanos. Pašreizējos apstākļos īpaša nozīme ir pacientu ar elpošanas ceļu tuberkulozi identificēšanai starp augsta riska grupām un pacientiem, kuri meklē medicīnisko aprūpi.
Pašlaik visiem pacientiem, kuri ir izgājuši uz ambulatoro klīniku un kuri pašreizējā gadā nav pārbaudīti ar rentgena metodi, kā arī personām, kurām ir augsts tuberkulozes risks, ir obligāta fluorogrāfija.
Riska grupu aptaujā prioritārais virziens ir pakāpeniska pāreja uz digitālās radiācijas tehnoloģiju, jo filmu fotofluorogrāfi neļauj iegūt labu tēlu un radīt ievērojamu radiācijas slodzi.
Īpaša paaugstinātas plaušu tuberkulozes riska grupa ir persona, kas saskaras ar pacientiem ar plaušu tuberkulozi. Tajā pašā laikā visbīstamākais ir tuvs ģimenes vai rūpniecisks kontakts ar baktēriju ekskrementiem.
Visbiežāk jutīgas pret plaušu tuberkulozi personas no šādām sociālajām grupām: BOMZHI, bēgļi, migranti, kas atbrīvoti no brīvības atņemšanas iestādēm, personas, kas dzīvo patversmēs, patversmēs, veco ļaužu aprūpes namos, narkoloģisko un psihiatrisko iestāžu pacienti.
Augsta riska grupa arī ietver tos, radioloģisku pazīmēm atlikuma pēc tuberkulozes izmaiņas plaušās un hilar limfmezgli kā calcifications, Fibrozo perēkļi, pleiras saaugumus vietām fibroze, kā arī jauniešiem ar hyperergic reakcijas uz Mantoux testā ar 2-L TE PPD.
Augsts tuberkulozes risks piemērota pacientiem ar dažādām blakus slimībām: profesionālā (putekļu), plaušu slimību, hronisku nespecifisku plaušu slimību (tai skaitā iedzimtu anomāliju), diabēts, kuņģa un divpadsmitpirkstu zarnas čūlu, sirds slimības ar asinsrites mazspēja (īpaši iedzimtu patoloģiju sirds), vēzi, hronisku alkoholismu un narkomāniju, kas inficēta ar HIV un cilvēkiem ar AIDS.
Liels risks saslimt ar tuberkulozi personām, kuras saņēma citotoksisku, kortikosteroīdu un staru terapiju, jauniem pacientiem, kuriem bija eksudatīvs pleirīts, sievietēm pēcdzemdību periodā un pēc aborta.
Riska grupas pacientiem sakarā ar samazinātu pretestību organisma tuberkulozes var attīstīties ļoti ātri (iespējams dažu nedēļu laikā, bet gandrīz noteikti 10 mēnešu laikā), tā, ka optimālais ilgums periodiskumu fluorogrāfija pārbaudēm nedrīkst pārsniegt 6 mēnešus. Tajā pašā laikā, klīnikās, kur pacientu grupas no riska grupas ir reģistrētas ambulatorā, jāizveido fluorokarte retrospektīvai plaušu patoloģijas novērtēšanai.
Galvenais uzdevums ir identificēt pacientus ar plaušu tuberkulozi, atbrīvojot ILO, jo šiem pacientiem parasti ir progresīva destruktīva tuberkulozes process, un tie ir ļoti epidemioloģiskās briesmas citiem.
Šādu pacientu ārstēšana ir gan klīnisko un epidemioloģisko nozīmi, jo tā ļauj ne tikai izvairīties no nāves progresiju TB, bet arī, lai apturētu izplatīšanos SDO, lai izvairītos attīstību hronisku procesa nepārtrauktu vai neregulāru izlaišanas.
Saistībā ar fluorogrāfisko pētījumu samazināšanu palielinās pareiza klīnisko simptomu novērtēšana un krēpu mikroskopiskā pārbaude pacienta stāvoklī.
Tuberkulozes noteikšanas pētījumu algoritms attēlots diagrammā: 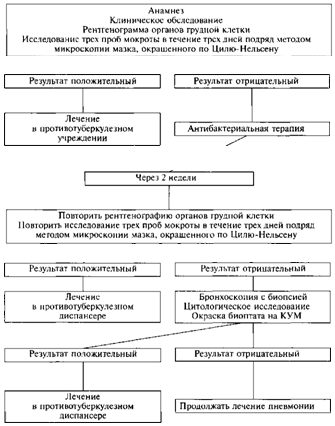
Visi pacienti, kuriem ir aizdomas par elpošanas ceļu tuberkulozi (Klepus vairāk nekā 2-3 nedēļas, klepus līdz asinīm, sāpes krūtīs, zemas kvalitātes un febrila temperatūra, svīšana naktīs, un svara zudums), Jums ir jābūt rentgenizmeklējumus, vispārējās asins un urīna analīzes un pārbaudīt krēpu uztriepes, ar mikroskopijas skābju baktērijas uztriepes ar krāsojumu uz Zilu-Nelsen.
Ārstēšanas dienā klīnikā vai pēc uzņemšanas slimnīcā pacientam ir jāizmanto krūšu kurvja rentgenogramma.
Krēpas mikroskopija jāīsteno visos klīniskās diagnostikas laboratorijas ārstniecības iestāžu vispārējo medicīnas tīkla (LU CHI): pieaugušo un bērnu slimnīcas, valsts, reģionālā, provinču, pilsētu un centrālā rajona slimnīcas, klīnikas, pētniecības institūti dažādās nozarēs, rajona slimnīcas un lauku veselības klīnikām, psihiatriskās slimnīcas, korektīvo darba iestāžu medicīnas un sanitārās vienības utt.
LU AKC klīniskajās diagnostikas laboratorijās ir jāpārbauda vismaz trīs krēpu uztriepes, izmantojot Zil-Nelsen mikroskopijas metodi skābju rezistentām mikobaktērijām.
No rīta ieteicams veikt krēpu testu trīs dienas pēc kārtas. Speciāli apmācītas medmāsas klātbūtnē pacientam jāapkaro krēpu.
Krēpu savākti ciešās stikla traukos ar platu kaklu un skrūvējamu vāciņu un jātransportē klīniskās diagnostikas laboratorijas slimnīcā, kur smērējumi ir izgatavotas un veic mikroskopija Ziehl-Nelsenu. Ja pacients nespēj saspiest krēpu, tad to var iegūt, izmantojot inhalatoru, kas izplata 3% hipertoniskā nātrija hlorīda šķīdumu.
Ja vismaz vienā no uztriepes tiek identificētas skābes izturīgas mikobaktērijas, tad pacients tiek pārnests uz antituberkulozes slimnīcu slimnīcu, kurai diagnosticēta plaušu tuberkuloze, MBT + specifiskai ārstēšanai.
Ja skābes izturīgas mikobaktērijas nav konstatētas trijās krēpās, tad pacients tiek ārstēts ar antibakteriālām zālēm, kā pneimonijā. Līdz ar to nav iespējams izmantot anti antibiotikas: streptomicīns, Kanamicīns, Amikacīns rifampicīnu, rifabutīnu, un gentamicīnu, kas nav saistītas ar anti-TB zāļu, bet kuru vāja bakteriostatisku iedarbību pret Office.
Pēc 2 nedēļām slimības, ja fons ir nespecifiska antibiotiku terapija nav atzīmēts pozitīvu klīnisku un rentgenoloģiski dinamiku procesā, pacients atkārtoti savākt trīs krēpu paraugus, trīs dienas pēc kārtas, lai uztriepes mikroskopijas metodi Ziehl-Nelsenu. Ja tiek konstatēts skābju rezistents MBT, vismaz vienā no krēpas uztriepēm pacients tiek pārnests uz TB slimnīcu.
Lai novērstu infekciju ar tuberkulozi, vācot krēpuĀrstam ir jāvalkā cepure, maska, eļļas apģērba priekšauts un gumijas cimdi. Jāievēro arī piesardzības pasākumi, uzglabājot un piegādājot krēpu laboratorijai pārbaudei. Uzglabāšanai un transportēšanai izmantojiet īpašus konteinerus vai metāla likmes.
Ja pirmie uztriepes bija pozitīvi, un pacients vēlreiz neatnāca pie ārsta, tas ir steidzami jāatrod un jāaicina veikt turpmāku izmeklēšanu, diagnozi un nodošanu ārstēšanai.
Dažos gadījumos (piemēram, ja pacients dzīvo tālu no medicīnas iestādes vai viņam ir grūti sasniegt viņu, vai viņa stāvoklis ir neapmierinošs), pacientu var hospitalizēt 2-3 dienas pārbaudei.
Dažās attālās vietās ir lietderīgāk apmācīt medicīnas asistentus vai citus paramedicīnus un dzemdību palīdzības stacijas (FAP), lai pareizi savāktu krēpu, saglabātu un ātri nogādātu to tuvākajā klīniskajā diagnostikas laboratorijā; personāls var tikt apmācīts arī krēpu uztriepju sagatavošanā, žāvēšanā, fiksēšanā un pēc tam nogādāšanā tuvākajā laboratorijā krāsošanai un pētniecībai.
Bērniem līdz 10 gadu vecumam, ņemot vērā krēpu iegūšanas grūtības, pārbauda kuņģa skalošanu vai balsenes tamponu. Procedūra tiek veikta agri no rīta tukšā dūšā, iegūtais saturs tiek savākts sterilā traukā un nosūtīts uz laboratoriju bakterioskopiskiem un kultūras pētījumiem.
Papildus krēpu mikroskopijai, kas krāsota ar Ziehl-Nelsen metodi, laboratorijas, kas aprīkotas ar luminiscējošiem mikroskopiem, var izmantot materiāla izpētei ar luminiscento mikroskopu.
Visiem pacientiem obligāti jāveic barības vielu krēpu kultūra, jo dažās no tām Biroju var noteikt tikai ar kultūras metodi.
Krēpas kultūra tuberkulozes izraisītāja ierosināšanai vai citai materiālai tiek veikta specializēta tuberkulozes iestāžu laboratorija. Ja iegūst pozitīvu rezultātu, visos gadījumos tiek veikta mikobaktēriju identifikācija un zāļu jutības noteikšana. Krēpu bakterioloģisko izmeklēšanu veic kā neatkarīgu pētījumu un vienlaicīgi ar krūšu starojuma diagnostiku.
Pacientu mikrobioloģiskā izpēte no riska grupām, kurām ir ilgstoša krēpu izdalīšanās, tiek veikta reizi gadā.
Krēpu mikroskopiskā pārbaude - vērtīga metode, kā identificēt visbīstamākās epidemioloģiski saistītās tuberkulozes formas cilvēkiem, kuriem ir ne tikai klepus, bet arī citi simptomi, kas raksturīgi elpošanas ceļu tuberkulozei. Tajā pašā laikā šī metode netiek uzskatīta par pilnīgi uzticamu, jo elpošanas tuberkuloze bieži nav simptomātiska.
Pat pacienti ar destruktīvu procesu un baktēriju izdalīšanos ilgu laiku saglabā savu darbību un nenovēro īstermiņa veselības pasliktināšanos, un, protams, LU OMS nesaņem medicīnisko palīdzību.
Maziem formas plaušu tuberkuloze, kā arī iespējamo baktēriju izdalīšanos, piemēram, tuberkulozes intratorakālajos limfmezglu ar fistulous formām trahejas un bronhu tuberkuloze, joprojām pastāv lielas iespējas slēpto slimības laikā netraucējot vispārējo veselību slimos. Šai sakarā pašlaik nav alternatīvu fluorogrāfijai, izvēloties cilvēkus ar plaušu patoloģiju.
Jāuzsver, ka ar krūškurvja orgānu fluorogrāfiju galvenokārt tiek konstatētas nelielas tuberkulozes formas, kas potenciāli apdraud citus kā progresējošu formu attīstības avotu ar baktēriju izdalīšanos.
Lielākā daļa pacientu ar destruktīvu procesu tiek atklāti starp tiem, kuri pieteikušies medicīniskajai aprūpei OU LHU, tomēr, kā minēts iepriekš, liels skaits cilvēku ar progresīvām formām var būt starp identificētajiem pacientiem. Šo situāciju var novērst, ja radiācijas testus veic ne tikai pacientiem, kuri dažādu iemeslu dēļ iekļūst slimnīcās, bet arī ambulatorā kontingenta gadījumā. Radioloģisko izmaiņu noteikšana plaušās ir pamats turpmākai izmeklēšanai.
Tuberkulīna diagnoze ir galvenā metode agrīna atklāšana tuberkulozes infekcija bērniem un pusaudžiem. Kā specifisku diagnostikas testu to izmanto bērnu un pusaudžu masu skrīningā tuberkulozei, kā arī klīniskajā praksē tās diagnosticēšanai. Šim nolūkam izmanto vienu intrakutānu tuberkulīna Mantoux testu ar diviem attīrītas Linnikova tuberkulīna tuberkulīna vienībām (TE) (2 TE PPD-L).
Viens no pieejamākajiem LU, AKM ir krūškurvja radiācijas izmeklēšanas metodes, krēpu un tuberkulīna diagnozes bakterioskopiska izpēte bērniem un pusaudžiem.
Visi nesen diagnosticētie pacienti ir sadalīti trīs grupās..
- Pirmā grupa - nekavējoties identificēti - pacienti ar komplikācijām primāro tuberkulozi (mazo formu primārais tuberkulozes sarežģītas un tuberkulozes intratorakālajos limfmezglu) un pacientiem ar ierobežotām procesos sekundārā Genesis (fokusa, infiltratīva un izplata plaušu tuberkulozes) šajā infiltrācijas fāzē, un bez jebkādām pazīmēm plaušu audu sabrukumu un baktēriju ekskrēcija, kā arī pleirīts. MBT noteikšana krēpās, izmantojot jebkuru pētījumu metodi, ja nav plaušu iznīcināšanas pazīmju, neizslēdz iespēju piešķirt pacientam tūlītēju identificēto grupu. Mūsdienu ķīmijterapija šajā pacientu grupā veicina veiksmīgu ārstēšanu ar pilnīgu specifisku pārmaiņu rezorbciju vai minimālu atlikušo izmaiņu veidošanos, kas samazina slimības atkārtošanās risku.
- Otra grupa - konstatēts vēlu - pacientiem ar smagām un hroniskām formām primāro tuberkulozi, kā arī slimniekiem ar kopīgām un akūti progresīvo tuberkulozes formu sekundārajā posmā sabrukuma uztriepes. Tuberkulozes šajā grupā pacientu bieži ir noteiktu recepti, destruktīvu procesu plaušās kopā ar uztriepes, pat apstākļos mūsdienu ķīmijterapijas izraisa lēnu kursu reparative procesiem. Klīniskā ārstēšana šajā pacientu grupā bieži vien ir saistīta ar lielu atlikušo izmaiņu veidošanos, kas nosaka slimības recidīva lielo varbūtību.
- Trešā grupa - atstāta novārtā vai novēlota, - pacientiem ar šķiedru-dobu un izplatītu tuberkulozi ar veidotiem dobumiem plaušās ar baktēriju izdalīšanos un augstu zāļu rezistences līmeni MW. Šī grupa ir visnelabvēlīgākā klīniskā, prognostiskā un epidemioloģiskā ziņā.
Galvenais gadījumu skaits, kas konstatēts pacienta sākotnējās ārstēšanas laikā ar ģimenes ārstu. Pacients, slikta pašsajūta, nekavējoties neprasīja ārsta palīdzību. Parādās zemfrekvences temperatūra līdz 37,5 C, pastāvīgi uzturēta. Pēc kāda laika savienojas sauss klepus, dažreiz ar flegmu ( smagi smēķētāji bieži nepievērš uzmanību tam, atsaucoties uz viņa slikto ieradumu). Un tad ir vērts uztraukties, ir pienācis laiks apmeklēt ārstu. Katrs ārsts apzinās plaši izplatīto tuberkulozes izplatību, tāpēc, ārstējot pacientu ar raksturīgiem simptomiem, viņam jājautā pacienta kontroles jautājumi, piemēram:
- Vai pacients iepriekš ir cietis no tuberkulozes?
- Vai viņa radinieki bija slimi ar tuberkulozi?
- Vai viņš bija saskarē ar tuberkulozes pacientiem?
- Tas, vai pacients nav reģistrēts pret tuberkulozes iestādē sakarā ar paaugstinātu jutību pret tuberkulīnu
- Vai tu iet ( un kad) pacienta plaušu fluorogrāfija
- Vai pacients atradās apcietinājumā vai saskarē ar cilvēkiem, kas iepriekš bija cietumā
- Vai viņš ir migrants, bezpajumtnieks, dzīvo nelabvēlīgos apstākļos un tā tālāk
Pēc anamnēzes savākšanas un rūpīgas pacienta izmeklēšanas dodas uz laboratorijas un instrumentālajiem pētījumiem.
Tuberkulīna diagnoze
Tā ir svarīga metode tuberkulozes diagnosticēšanai, papildinot pacienta klīnisko pārbaudi. Tas norāda uz paaugstinātu specifisko ķermeņa jutību, ko izraisa BCG vakcīna vai tuberkulozes izraisītājs ( mikobaktēriju tuberkuloze). Tuberkulīna testam izmanto tuberkulīnu - ūdens glicerīna ekstraktu, kas izolēts no patogēna kultūras. Tuberkulīns veselīgu ķermeni neizraisa sensibilizāciju un arī nespēj attīstīties pret tuberkulozi. Atbilde uz tuberkulīnu attīstās tikai bērniem, kas iepriekš bijuši sensibilizēti bCG vakcīna vai patogēna baktēriju.
Mantoux tests: Nelielu ādas virsmu uz apakšdelma iekšējās virsmas, proti, apakšdelma vidējo trešdaļu, apstrādā ar etilspirtu. Adatu injicē intrakutāli, paralēli ādas virsmai, nogriežot adatu uz augšu. Tiek injicēts 0,1 ml tuberkulīna, kas ir viena tā deva. Tuberkulīna ievadīšanas vietā ādā veidojas mazs ( diametrs 7-8 mm) bālgans krāsu burbulis citrona mizas veidā. Ir ļoti svarīgi, lai speciāli apmācīta medmāsa veiktu Mantoux testu, jo ar nepareizu izpildes metodi rezultāti kļūst neuzticami. Paraugu rezultātus novērtē 72 stundas pēc testa. Novērtējumu veic ārsts vai speciāli apmācīta medmāsa. Pirmkārt, pārbaudiet apakšdelmu tuberkulīna injekcijas vietā. Tātad jūs varat atklāt ārējās reakcijas pazīmes, ādas apsārtumu vai infiltrācijas uzkrāšanos.
Nelielu ādas virsmu uz apakšdelma iekšējās virsmas, proti, apakšdelma vidējo trešdaļu, apstrādā ar etilspirtu. Adatu injicē intrakutāli, paralēli ādas virsmai, nogriežot adatu uz augšu. Tiek injicēts 0,1 ml tuberkulīna, kas ir viena tā deva. Tuberkulīna ievadīšanas vietā ādā veidojas mazs ( diametrs 7-8 mm) bālgans krāsu burbulis citrona mizas veidā. Ir ļoti svarīgi, lai speciāli apmācīta medmāsa veiktu Mantoux testu, jo ar nepareizu izpildes metodi rezultāti kļūst neuzticami. Paraugu rezultātus novērtē 72 stundas pēc testa. Novērtējumu veic ārsts vai speciāli apmācīta medmāsa. Pirmkārt, pārbaudiet apakšdelmu tuberkulīna injekcijas vietā. Tātad jūs varat atklāt ārējās reakcijas pazīmes, ādas apsārtumu vai infiltrācijas uzkrāšanos.
 Sarkano ādu nedrīkst sajaukt ar infiltrātu. Lai to izdarītu, ir jāsalīdzina apakšdelma ādas kroku biezums veselā vietā un pēc tam adatas ievietošanas vietā. Atšķirība ir tāda, ka tad, kad kroku apsārtums saglabājas tādā pašā biezumā un infiltrācijas laikā, virs tuberkulīna injekcijas vietas sabiezē locītavu biezumu. Pēc ārējas pārbaudes reakcijas diametrs tiek mērīts, izmantojot caurspīdīgu lineālu.
Sarkano ādu nedrīkst sajaukt ar infiltrātu. Lai to izdarītu, ir jāsalīdzina apakšdelma ādas kroku biezums veselā vietā un pēc tam adatas ievietošanas vietā. Atšķirība ir tāda, ka tad, kad kroku apsārtums saglabājas tādā pašā biezumā un infiltrācijas laikā, virs tuberkulīna injekcijas vietas sabiezē locītavu biezumu. Pēc ārējas pārbaudes reakcijas diametrs tiek mērīts, izmantojot caurspīdīgu lineālu.
Ir trīs veidu reakcijas uz tuberkulīnu:
1.
Negatīva reakcija
- raksturīga pilnīga apsārtuma un infiltrācijas neesamība ( 0-1 mm).
2.
Apšaubāma reakcija
- dažādu izmēru ādas apsārtums vai infiltrācija, kuras diametrs ir 2 - 4 mm /
3.
Pozitīva reakcija
- obligāta infiltrāta klātbūtne ar diametru 5 mm vai vairāk.
Savukārt pozitīvās reakcijas var iedalīt vairākos veidos atkarībā no infiltrāta diametra:
- Vāji pozitīvi - 5 - 9 mm.
- Vidējā intensitāte - 10-14 mm.
- Izrunāts - 15 - 16 mm.
- Hiperergiska - bērniem un pusaudžiem 17 mm vai vairāk un pieaugušajiem no 21 mm. Šajā kategorijā ietilpst arī ādas virulogēnās reakcijas.
- Pastiprināta reakcija, kam seko infiltrācijas palielināšanās par 6 mm vai vairāk, salīdzinot ar iepriekšējo paraugu.
 1.
Krēpas savākšana un apstrāde: Procedūra tiek veikta speciāli sagatavotā telpā, prom no neatļautām personām. Visizplatītākā metode ir ņemt materiālu no balsenes ar tamponu. Gļotas tiek savāktas klepus vai krēpas atsegšanas laikā. Tamponu ievieto speciālā noslēgtā traukā un nekavējoties nosūta mikrobioloģiskai pārbaudei. Tāda pati materiālu kolekcija, kas iegūta, pētot bronhu un / vai kuņģa mazgāšanas ūdeni, pētot smadzeņu šķidrumu, pleiras šķidrumu, bronhoskopiju, pleiras biopsiju, plaušu biopsiju.
1.
Krēpas savākšana un apstrāde: Procedūra tiek veikta speciāli sagatavotā telpā, prom no neatļautām personām. Visizplatītākā metode ir ņemt materiālu no balsenes ar tamponu. Gļotas tiek savāktas klepus vai krēpas atsegšanas laikā. Tamponu ievieto speciālā noslēgtā traukā un nekavējoties nosūta mikrobioloģiskai pārbaudei. Tāda pati materiālu kolekcija, kas iegūta, pētot bronhu un / vai kuņģa mazgāšanas ūdeni, pētot smadzeņu šķidrumu, pleiras šķidrumu, bronhoskopiju, pleiras biopsiju, plaušu biopsiju. 2.
Sputum mikroskopija: 
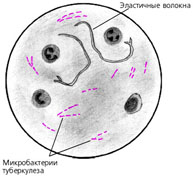 Tā ir ātrākā un lētāka metode Mycobacterium tuberculosis noteikšanai. Metode balstās uz mikobaktēriju spēju saglabāt savu krāsu pat pēc apstrādes ar dažādiem skābes šķīdumiem. Tātad, tie tiek konstatēti ar mikroskopu iekrāsotajās krēpās. Kopā ar vienkāršu mikroskopiju tiek izmantota fluorescences mikroskopija, kuras pamatā ir ultravioleto staru izmantošana mikobaktēriju noteikšanai.
Tā ir ātrākā un lētāka metode Mycobacterium tuberculosis noteikšanai. Metode balstās uz mikobaktēriju spēju saglabāt savu krāsu pat pēc apstrādes ar dažādiem skābes šķīdumiem. Tātad, tie tiek konstatēti ar mikroskopu iekrāsotajās krēpās. Kopā ar vienkāršu mikroskopiju tiek izmantota fluorescences mikroskopija, kuras pamatā ir ultravioleto staru izmantošana mikobaktēriju noteikšanai.
Molekulārās ģenētiskās metodes mikobaktēriju tuberkulozes diagnosticēšanai 1. Polimerāzes ķēdes reakcija: ir mikobaktēriju tuberkulozes ģenētiskā materiāla atšifrējums. Paredzēts, lai atklātu krēpas izraisītāju un atpazītu baktēriju daudzveidību. Metode ir īpaši jutīga un specifiska.
2.
Patogēnu zāļu rezistences noteikšana
Uzskata, ka tie Mycobacterium tuberculosis celmi, kuriem šī medikamenta bakteriostatiskā vai baktericīdā iedarbība ir minimāla, ir jutīgi pret kādu konkrētu narkotiku.
Minētos mikobaktēriju celmus, kas var vairoties, ja tie tiek pakļauti zāļu iedarbībai minimālā vai paaugstinātā koncentrācijā, sauc par rezistentiem vai rezistentiem pret šo narkotiku.
3.
Seroloģiskās metodes tuberkulozes diagnostikai
Seroloģiskās metodes asins plazmas komponentu pētīšanai ir balstītas uz daudzu ar tuberkulozi saistītu antigēnu noteikšanu, kā arī uz dažādām imūnreakcijām, ko izraisa dažādas tuberkulozes formas.
4.
Asins analīze
Hemoglobīns un eritrocīti vairumā gadījumu paliek nemainīgi, izņemot gadījumus, kad ir akūta asins zudums. Indikators, kas norāda uz aktīva tuberkulozes procesa klātbūtni, ir eritrocītu sedimentācijas ātrums. Paātrināta ESR ir raksturīga ne tikai svaigai aktīvai tuberkulozei, bet arī hroniska procesa saasināšanai.
Atlikušie asins analīzes rādītāji ievērojami atšķiras atkarībā no plaušu bojājumu veida.
5.
Urīna analīze
Analizējot urīnu pacientam ar plaušu tuberkulozi, nav vērojamas būtiskas novirzes no normas. Izmaiņas notiek tikai tuberkulozes bojājumos un urīnceļos.
6.
Rentgenstaru diagnostikas metodes
 Visbiežāk izmantotās metodes plaušu tuberkulozes diagnosticēšanai ir šādas metodes:
Visbiežāk izmantotās metodes plaušu tuberkulozes diagnosticēšanai ir šādas metodes:
- Radiogrāfija
- Roentgenoscopy
Fluorogrāfija- Tomogrāfija
- Tracheobronhoskopija
- Bronchoscopic Lavage
- Torakoskopija ( pleuroskopija)
- Transbronču biopsija
- Transthoracic adatas biopsija
- Pleiras punkcija un pleiras biopsija
Savlaicīga un novēlota tuberkuloze
Lai pilnībā un ātri izārstētu tuberkulozi, tās savlaicīga atklāšana ir ļoti svarīga. Agrīna diagnoze slimības sākumposmā var novērst tā tālāku izplatīšanos, un tas ir arī būtisks elements tuberkulozes infekcijas profilaksei. Tuberkulozi, kas atklāta vēlu attīstības stadijās, ir ļoti grūti ārstēt. Turklāt šādi pacienti kļūst epidēmiski bīstami citiem.
V.Yu. Mishin
Tuberkulozes diagnostika ietver vairākus secīgus posmus. Turklāt visas pētniecības metodes ir iedalītas 3 grupās: obligāto diagnostikas minimumu (ODM), papildu neinvazīvas pētniecības metodes (DMI-1) un invazīva (DMI-2) un beidzot izvēles metodes (PMI).
ODM ietver sūdzību izpēti, slimības un dzīvības anamnēzi, asins un urīna klīniskās analīzes, krēpu mikroskopiju saskaņā ar Zil-Nelsen vismaz trīs paraugus ar kvantitatīvu novērtējumu par baktēriju masu, krūšu orgānu rentgenstaru frontālās un sānu projekcijās un Mantoux testu ar 2 TE PPD-L .
Uz DMI-1 jāiekļauj paplašināta mikrobioloģiskā diagnostika ar krēpu pārbaudi, izmantojot PCR un krēpu kultūru barības vielās, nosakot MBT zāļu rezistenci pret zālēm pret tuberkulozi, kā arī krēpu kultūru uz nespecifiskām mikroflorām un sēnēm; padziļināta radiācijas diagnostika, izmantojot plaušu un mediastīna CT skenēšanu, ultraskaņu pleirītam un subpleurāli izvietotiem noapaļotiem veidojumiem; padziļinātas imūndiagnostikas metodes, lietojot enzīma imūnanalīzi (ELISA), lai atklātu pret tuberkulozes antivielas (AT) un antigēnus (AH) asinīs.
Papildus krēpu mikroskopijai un citam patoloģiskajam materiālam kā obligātajam diagnostikas minimumam ir iespējams pētīt ar luminiscentās mikroskopijas, PCR un bakterioloģiskās (kultūras) metodes barības vielu vidē, ko veic specializētās tuberkulozes iestāžu laboratorijās.
MBT noteikšana ļauj noteikt etioloģisko diagnozi bez lielām grūtībām. Visgrūtākā situācija tuberkulozes diagnosticēšanā ir pacientiem ar klīniskiem simptomiem, ja nav krēpu, kā arī tad, kad krēpās MBT nav konstatēts. Šādos gadījumos plaušu tuberkulozes diagnoze lielā mērā balstās uz radiācijas metodēm krūšu orgānu pārbaudei.
Šīs metodes papildina pacientu klīniskās izpētes rezultātus, savukārt to apvienotā analīze ļauj paaugstināt jutīgumu un specifiskumu, un ar mikrobioloģisko un morfoloģisko pētījumu negatīviem datiem ir izšķiroša nozīme. X-ray CT skenēšana plaušās ir vadošā diagnostikas metode.
Plaušu tuberkulozes rentgena tomogrāfiskais attēls atšķiras polimorfismā gan infiltrējošo izmaiņu rakstura dēļ, gan specifisku izmaiņu lokalizācijā, un tai ir nepieciešama mērķtiecīga diferenciāldiagnoze.
Specifiskam tuberkuloza iekaisumam ir dažādas radiogrāfiskas izpausmes - no viena vai vairākiem saplūstošiem fokusiem, noapaļotiem infiltrātiem un pereissuritov līdz lobaram tuberkulozes pneimonijā. Tomēr lielāko daļu izpausmju raksturo procesa lokalizācija apikālajos [C1], aizmugurējos [C2] un augšējos plaušu segmentos.
Visus plaušu variantus raksturo ne tikai kontrastējošo un infiltrējošo ēnu klātbūtne, bet arī diezgan bieži - dobumi, kas parasti ir saistīti ar bronhogēnu izplatīšanos, kam ir noteiktas likumsakarības, kas var kalpot par diagnostikas zīmi.
Kreisās plaušu augšējās daivas dobuma klātbūtnē kreisās plaušu apakšējās daas apakšējās daivas centrālās daļas un priekšējās [C3], augšējo niedru, apakšējo mēles segmentu, kā arī bazālo, priekšējo basālo, sānu pamatu [C9] un aizmugures bazālo [C10] segmentu klātbūtne. .
Labās puses dobumos izplatīšanās fokusējas uz augšējās daivas apakšējām daļām ar dominējošo priekšējā [C3] segmenta bojājumu, un arī kreisajā plaušā notiek krustmetastāzes, galvenokārt augšējos niedros un apakšējos niedru segmentos.
Klīniskajā praksē mantoux testa diagnostiskā vērtība ar 2 TE PPD-L pieaugušiem pacientiem ar radioloģiski nosakāmām plaušu izmaiņām nosaka tās negatīvā vai hiperergiskā reakcija. Pacienta klātbūtnē negatīva reakcija Mantoux (injekcijas injekcijas vietā) plaušu pārmaiņas biežāk attiecas uz procesiem, kas nav tuberkuloze.
Hiperergiskas reakcijas klātbūtnē (papila izmērs 21 mm vai vairāk diametrā vai vezikulāras nekrotiskas reakcijas neatkarīgi no papulas lieluma) plaušu pārmaiņas biežāk ir tuberkulozas.
Pozitīvai Mantoux 2 TE PPD-L reakcijai ar papīra izmēru 5 d0 20 mm diametrā nav diagnostikas vērtības, jo vairāk nekā 70% pieaugušo iedzīvotāju vecumā līdz 30 gadiem jau ir inficēti.
Pašlaik izmantotās laboratorijas un imunoloģiskās metodes plaušu tuberkulozes diagnosticēšanai galvenokārt ir netiešas un tiek izmantotas visaptveroši, lai palielinātu diagnozes pārbaudes nozīmi.
Gadījumos, kad plaušu tuberkulozes izmaiņas ir apšaubāmas, varat izmantot terapiju ar exjuvantibus. Tajā pašā laikā ķīmijterapija tiek nozīmēta ar četrām pret TB ārstētām zālēm (izoniazīds, rifampicīns, pirazinamīds un etambutols). Šādos gadījumos pēc 2 mēnešiem ir nepieciešama otrā rentgena izmeklēšana.
Tuberkulozes etioloģijas slimības gadījumā novērojama daļēja vai pilnīga iekaisuma izmaiņu rezorbcija - tā ir tā sauktā aizkavēta diagnoze. Līdz tam laikam ir iespējams iegūt barības vielu krēpu kultūras rezultātus, kas veikti pirms ķīmijterapijas uzsākšanas. Kultūras pieaugums MBT klātbūtnē materiālā parasti tiek atzīmēts pēc 4-8 nedēļām, kas kalpo par diagnozes apstiprinājumu.
DMI-2 ietver bronhoskopiju dažādām sugām biopsijas (aspirācija, suka utt.) un BAL; pleiras dobuma un pleirobiopijas punkcija; transsthoracic plaušu biopsija; torakoskopija, mediastinoskopija un, visbeidzot, atklāta plaušu biopsija, kam seko iegūto materiālu citoloģiskie, histoloģiskie un mikrobioloģiskie pētījumi.
Speciālu tuberkulozes granulomas (kazeozes, epitelioīda un daudzslāņu šūnu) elementu noteikšana biopsijā ļauj morfoloģiski pārbaudīt plaušu tuberkulozi un nekavējoties sākt pret tuberkulozes ārstēšanu.
PMI ļoti daudz un tie ir vērsti ne tikai uz tuberkulozes diagnosticēšanu, bet arī uz dažādu iekšējo orgānu un vielmaiņas procesu funkcionālā stāvokļa noteikšanu. Pārbaudiet glikozes līmeni asinīs, aknu darbību, sirds un asinsvadu sistēmu, elpošanas funkciju, asins gāzu sastāvu, plaušu asinsriti utt.
